AGC Research Report 74(2024)
少量の酸化リチウムを添加したバリウムシリケートガラスの結晶化挙動
Crystallization behavior of BaO-SiO2 glasses with a small amount of Li2O
梶原貴人*
Takato Kajihara
*AGCテクノグラス株式会社 技術センター(takato.kajihara@agc.com)
結晶化ガラスはガラスと結晶の特性を併せ持ち、優れた機械特性や誘電特性、熱物性などを発現できる材料である。結晶化ガラスは、一般的にガラス転移点以上の温度でガラスを熱処理し結晶相を析出させ作製される。そのため、カーボンニュートラルや省エネルギーの観点からは低温・短時間の熱処理で結晶化できるガラス組成が望ましい。そこで本報告では、酸化リチウムの添加によるバリウムシリケートガラスの結晶化の促進効果に着目した。xLi2O-(30-x)BaO-70SiO2[ mol%](x = 0, 0.2, 0.5)のガラスについて熱処理に伴う微細構造変化を調査した結果、酸化リチウムの添加量に伴い結晶化挙動が大きく変化することが分かった。酸化リチウム無添加のガラスでは結晶化初期に単斜晶系のBa2Si4O10(H-BaSi2O5)の準安定相が生成するのに対し、酸化リチウム添加ガラスは、熱処理初期においてガラスがシリコンリッチなドロップレット相とバリウムリッチなマトリックス相に分相することが分かった。酸化リチウム添加ガラスでは、熱処理初期において分相が生じることでマトリックス相のガラス組成がSanbornite(BaSi2O5)の化学量論組成である33.3BaO-66.7SiO2[mol%]に近づき結晶化が促進されたものと考えられ、結晶化促進効果は0.2 mol%と少量の酸化リチウムの添加でも確認することができた。
Glass-ceramics are excellent materials with both glass and crystalline properties, such as mechanical properties, dielectric properties, and thermophysical properties. Generally, a glass-ceramic is produced by the heat treatment of a mother glass at a temperature above the glass transition temperature to precipitate crystalline phases. However, for carbon neutrality and energy conservation, glasses that can be crystallized by low-temperature heat treatment in short periods are desirable. Therefore, this study aims to investigate the crystallization behavior of barium silicate glass, with the addition of lithium oxide, which reportedly promotes crystallization. The microstructural changes of xLi2O–(30-x)BaO–70SiO2[mol%](x = 0, 0.2, and 0.5)glasses during heat treatment were investigated. In a glass without lithium oxide, a metastable phase of monoclinic Ba2Si4O10(H-BaSi2O5), which is a crystalline phase of the barium silicate system, was formed in the early stage of crystallization. Conversely, in the glass containing lithium oxide, phase separation occurred in the early stages of heat treatment, forming a silicon-rich droplet phase and a barium-rich matrix phase. The crystallization of the barium silicate glass system was promoted by the change in the glass composition of the matrix phase to a composition close to the stoichiometric composition of Sanbornite(BaSi2O5)because of the occurrence of the phase separation.
1. 緒言
結晶化ガラスはガラス中に結晶を含有する材料であり、母材となるガラス組成や作製方法によって析出する結晶相やそのサイズ分布が変化するために、様々な機能を発現できる。結晶化ガラスは、この特徴を活かし、調理用のクックトップや耐熱食器、歯科部材、建築部材のような身近なものから、超大型望遠鏡のミラーやミサイル用のレドームまで様々な用途に用いられている(1)。
結晶化ガラスの一般的な作製方法として、ガラスを熱処理し、一部を結晶化する方法(1)が挙げられる。結晶化は、板状や粉末状のガラスをガラス転移温度(Tg)以上に加熱することで、結晶核が生成し、結晶相の生成と成長が進行する(1)。ガラス組成によっては1000 ℃以上と高温で長時間の熱処理を行うこともあるため、カーボンニュートラルや省エネルギーの観点からは低温・短時間での結晶化処理が可能なガラス組成が求められる。そのためには、ガラスにおける結晶化促進のメカニズムを理解し、組成設計や熱処理方法に反映させることが重要である。
そこで結晶化促進のメカニズム解明のために、酸化リチウムを添加することで結晶化の促進が報告されているバリウムシリケートガラスに着目した(2,3)。33.3BaO-66.7SiO2[ mol%]ガラス(以降BS2ガラス)は、結晶核の生成を促す核生成剤を添加することなく内部核生成が生じ、体積結晶化が可能な数少ないシリケートガラスである(4)。このBS2ガラスでは、Sanbornite(BaSi2O5)(5)と呼ばれる結晶相が生成することが知られている。この結晶相には、単斜晶系で高温相のBa2Si4O10(H-BaSi2O5)と直方晶系で低温相のBaSi2O5(L-BaSi2O5)の2種類の構造(6,7)が存在し、ガラス中で生成する場合は初めに高温相のH-BaSi2O5が生成し、熱処理温度の上昇や、熱処理時間の増加に伴って低温相であるL-BaSi2O5へ相変態すると報告されている(2,4,8)。
BS2ガラスの組成はBaSi2O5の化学量論組成と同じであり、核生成速度がBaO-SiO2 2元系ガラスの中で最も大きいことが報告されている(4,9,10)。Rowlandsらは、このBS2ガラスに酸化リチウムを導入すると、核生成温度の低温化やH-BaSi2O5からL-BaSi2O5への相変態が急速に生じることを報告しており、酸化リチウム添加の効果は結晶化促進の観点で注目すべきである(2,3)。Rowlandsらの検討では3.3Li2O-30BaO-66.7SiO2[mol%]のガラスが最も酸化リチウムの添加量が低い組成であり、3.3mol%以下の酸化リチウム添加量のガラスに対する検討は行われていない。そこで本研究では、さらに少量の酸化リチウムを添加することによって結晶化が促進するかを調査するとともに、熱処理に伴う微細構造変化から結晶化促進のメカニズムを明らかにすることを目的とした。
2. 実験方法
2.1. ガラス母材の作製と熱処理方法
結晶化前のガラス母材として、xLi2O-(30-x)BaO-70SiO2[ mol%](x = 0, 0.2, 0.5)の3種類を作製した。BS2ガラスはBaSi2O5の化学量論組成と同じ組成であるのに対し、本研究で扱うガラスは結晶化促進の効果が強調されるようにBS2ガラスに対して酸化バリウムが少なく、二酸化ケイ素の多い組成とした。それぞれのサンプル名は酸化リチウム添加量と対応させLBS0、LBS0.2、LBS0.5とした。
原料は珪砂(株式会社山森土本鉱業所、純度99.9%)、炭酸リチウム(関東化学株式会社、純度99%)、炭酸バリウム(関東化学株式会社、純度99%)を用いた。原料溶解中に発生する泡の脱泡には、清澄剤として硫酸塩をSO3換算で0.1wt%添加した。硫酸塩源は、LBS0では硫酸バリウム(関東化学株式会社、純度不明)、LBS0.2とLBS0.5では硫酸リチウム一水和物(関東化学株式会社、純度99%)を使用した。ガラス量で400gになるように原料を調整した後、白金るつぼを用いて大気雰囲気下の電気炉にて1600℃で原料を溶解し、白金スターラーで融液の撹拌を行った。その後、融液を室温のカーボン板上に流しだし、冷却用の電気炉にてLBS0:735℃、LBS0.2:720℃、LBS0.5:700℃で3時間保持した後、0.5℃/minの条件で冷却することでガラスブロックを作製した。
得られたガラスブロックは30mm × 30mmのサイズに切断し、サンプルの厚みが2mmになるように横型平面研削機を用いて1000番の砥石で精密研磨を行った。加工後のガラス板は、電気炉を用いて室温から表1に示す熱処理温度まで5℃/minで昇温し、熱処理温度に到達後、所定の時間保持を行い、5℃/minで室温まで降温した。熱処理温度は後述する示差走査熱量測定(DSC:Differential Scanning Calorimetry)(11)より決定した。

2.2. ガラス母材および熱処理後のガラスの評価
作製したガラス母材をアルミナ乳鉢およびアルミナ乳棒を用いて粉砕した後、ふるいを用いて粒子径(D)が106 μm≦D≦180 μmの粉末を得た。その後、直径5.0mm、高さ5.0mmの白金パンに約70mgのガラス粉末をいれ、示差走査熱量計(Bruker AXS社製、DSC 3300SA)でDSC測定を行った。DSC測定の際の昇温速度は10℃/minとし、室温から1000℃まで測定した。DSC測定結果から熱分析システム解析ソフト(NETZSCH JAPAN社製)を用いて、ガラス転移点:Tg、結晶化開始温度:T0、結晶化ピーク温度:Tcをそれぞれ求めた。なお、DSCのベースラインが吸熱側にシフトする温度をTgと定義した。
熱処理後のサンプルは横型平面研削機を用いて1000番の砥石で精密研磨を行った後、酸化セリウムのスラリーを研磨剤に用いた仕上げ研磨を行うことで厚みが0.5mmのサンプルを得た。加工後の熱処理サンプルは、顕微レーザーラマン分光測定装置(株式会社堀場製作所製、LabRAM HR Evolution)を用いて励起波長:532nm、グレーティング:1200gr/mm、対物レンズ:100倍の条件で200 ~ 1200cm-1の範囲でラマン分光測定を行った。加工後の熱処理サンプルをアルミナ乳鉢およびアルミナ乳棒を用いて粉砕し、X線回折(X-ray Diffraction:XRD)測定と走査透過電子顕微鏡(Scanning Transmission Electron Microscopy:STEM)観察に供した。
XRD測定はX線回折装置(株式会社リガク製、Smart Lab)を使用した。粉末サンプルを試料ホルダーにセッティングし、Cu-Kα線源を用いて管電圧:45kV、管電流:200mA、測定角度範囲2θ:10 ~40°、ステップ幅:0.020°の条件でXRD測定を実施した。測定結果はハナワルト法(12)を用いてInorganic Crystal Structure Database(ICSD)に収録されている結晶相の回折強度データと比較することで結晶相の同定を行った。
STEM観察用のサンプルは粉砕して得たサンプル粉末をエタノール中に分散させ、カーボン支持膜付きのCu グリッド(EM Japan株式会社製、quantifoilR0.6/1 200mesh)上に滴下し、自然乾燥させた。その後、導電性を上げるためにカーボンをコーティングした。カーボンコーティング後のサンプルは、収差補正走査透過電子顕微鏡(Thermo Fisher Scientific社製、Titan Cubed G2 60-300)を用いて、加速電圧:300kVでSTEM観察、エネルギー分散型X線分光法(EDS:Energy Dispersive X-ray Spectroscopy)、4次元走査透過電子顕微鏡法(4D-STEM)(13)を実施した。STEM観察時には高角度散乱暗視野(HAADF:High Angle Annular Dark-Field)像を検出器の取り込み角:52 ~ 200mrad、カメラ長:115mmの条件で取得した。シリコン、バリウム、酸素の組成分析を同装置に備え付けられているEDS分析装置Super-Xを用いて収束半角:18mrad、プローブ電流:70pA、プローブ直径:0.1nm未満、ステップサイズ:4nmの条件で実施した。また、4D-STEM法を用いて任意の領域の電子回折パターンを取得した。4D-STEM像の取得条件は、プローブ電流:10pA未満、収束半角:1.2mrad、エネルギーフィルター:ゼロロスピークを含む ±5eVのエネルギー範囲とし、試料上でのビームスキャンのステップサイズ:2nm、各回折パターンの解像度:0.171nm-1/ピクセル、二次元実空間での測定点あたりの露光時間:0.05秒とした。
3. 実験結果
3.1. 熱処理前のガラスの熱分析
図1に昇温速度:10℃/minにおける熱処理前のガラス粉末のDSC測定結果(14)を示す。LBS0とLBS0.2に着目すると、LBS0では820 ~ 920℃、LBS0.2では800 ~ 850℃でそれぞれ2つの発熱ピークが重なって存在しており、本研究では発熱量の大きなピーク温度(図中の青矢印部)を最大結晶化ピーク温度(Tc)とした。Tcの発熱ピークに注目すると酸化リチウム無添加のLBS0の発熱ピークはブロードであり、酸化リチウムの添加量が増えるにつれて発熱ピークはシャープになっている。また、酸化リチウム添加量の増加にともないTg、T0、Tcはそれぞれ低温側にシフトしている。表2にDSC 測定結果より求めたTg、T0、Tcと、T0以降の発熱ピークの温度(T1 ~ T5)、T0とTgとの差分温度:T0 - Tg、TcとT0との差分温度:Tc - T0の一覧(14,15)を示す。T0 - Tgはガラス転移点から結晶化開始までの温度であるため、この値が大きいほどガラスとして安定であることを示している。Tc - T0は結晶化開始温度から最大結晶化ピーク温度までの温度であるため、この値が小さいほど最大結晶化ピークに起因する結晶相が生成しやすいことを示している。酸化リチウムの添加量が増えるにつれてT0 - Tgが大きくなり、Tc - T0が小さくなっていることがわかる。
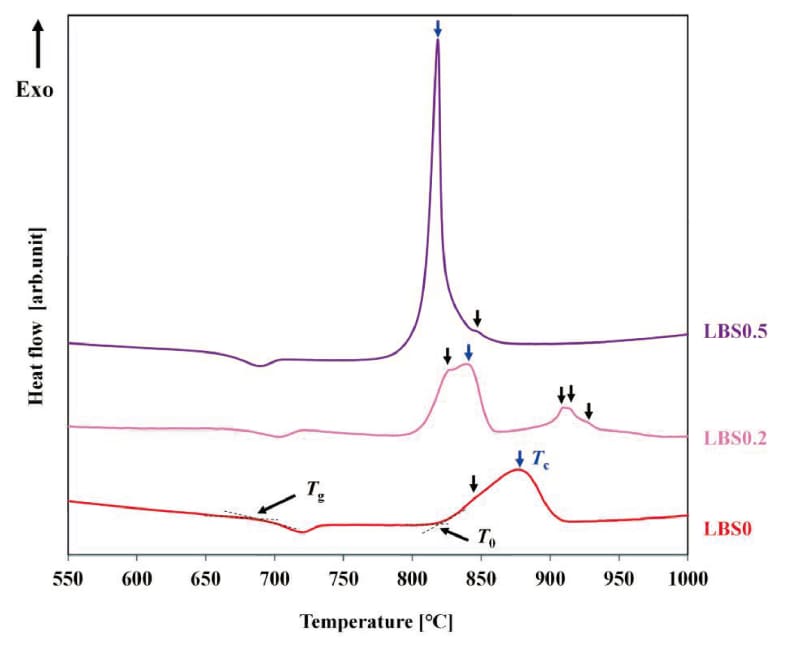 Fig.1 Non-isothermal DSC curves of LBSx glass heated at 10℃ /min(14). Particle sizes are over 106 μm and less than 180 μm. The arrows in the figure indicate the exothermic peaks, and the blue arrows indicate each maximum crystallization peak.
Fig.1 Non-isothermal DSC curves of LBSx glass heated at 10℃ /min(14). Particle sizes are over 106 μm and less than 180 μm. The arrows in the figure indicate the exothermic peaks, and the blue arrows indicate each maximum crystallization peak.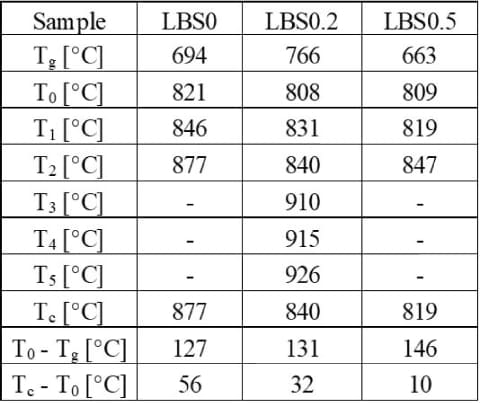
3.2. 熱処理サンプルのX線回折測定
図2にTc近傍の温度で30分間保持を行ったサンプルのXRD測定結果(15)を示す。図中の下部にICSDより取得した代表的なバリウムシリケート系結晶相(6,16,17)の回折ピークを示している。LBS0とLBS0.2のX線回折パターンより、一部の回折ピークを除いてブロードな回折ピークが多く確認できる。この回折パターンの形状はBS2ガラスの結晶化初期過程で生成が報告されているH-BaSi2O5の準安定相(Metastable H-BaSi2O5:M-BaSi2O5と呼称する) のそれと類似している(8)。また、LBS0のX線回折パターンからBa5Si8O21やBa6Si10O26の回折ピークと近い角度にピークが確認できる。これらの結晶相はBS2ガラスの結晶化初期過程での生成が報告されている結晶相(18-23)であるが、LBS0.2では確認できない。一方、LBS0.5ではLBS0やLBS0.2のようなブロードな回折ピークは確認できず、L-BaSi2O5と対応する回折ピークとわずかに二酸化ケイ素の結晶相であるCristobaliteと考えられる回折ピーク(図中のxマーク)が確認できる。
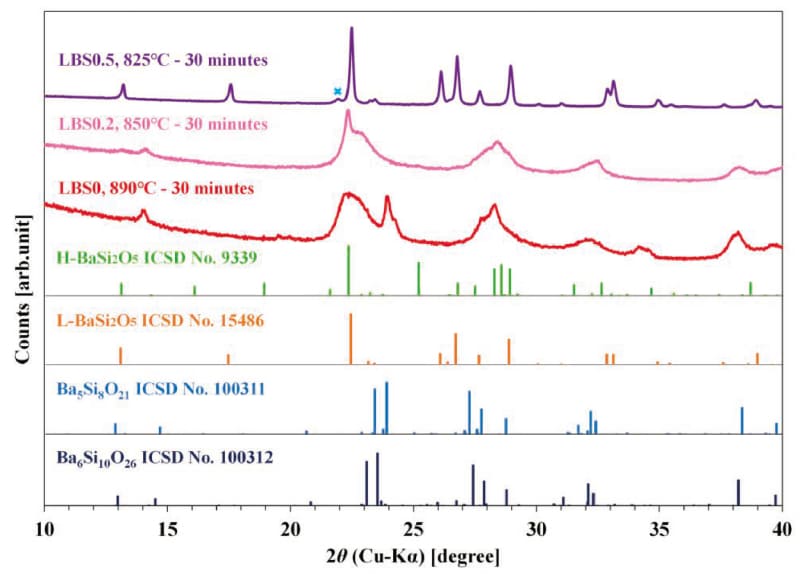 Fig.2 Comparison of XRD patterns in LBSx glasses heat-treated at near Tc for 30 minutes(15). The diffraction patterns of L-BaSi2O5, H-BaSi2O5, Ba5Si8O21 and Ba6Si10O26 are shown as references. The cross mark in the figure indicates diffraction peak that is thought to be cristobalite(ICSD No. 75300).
Fig.2 Comparison of XRD patterns in LBSx glasses heat-treated at near Tc for 30 minutes(15). The diffraction patterns of L-BaSi2O5, H-BaSi2O5, Ba5Si8O21 and Ba6Si10O26 are shown as references. The cross mark in the figure indicates diffraction peak that is thought to be cristobalite(ICSD No. 75300).図3にTc近傍の温度で24時間の保持を行ったサンプルのXRD測定結果(15)を示す。LBS0は、その処理温度が890℃と最も高温であるにも関わらず、24時間の保持でもL-BaSi2O5は確認できず、H-BaSi2O5とみられる回折ピークが確認できる。LBS0.2とLBS0.5ではL-BaSi2O5とみられる回折ピークとCristobaliteとみられる回折ピークが確認できる。
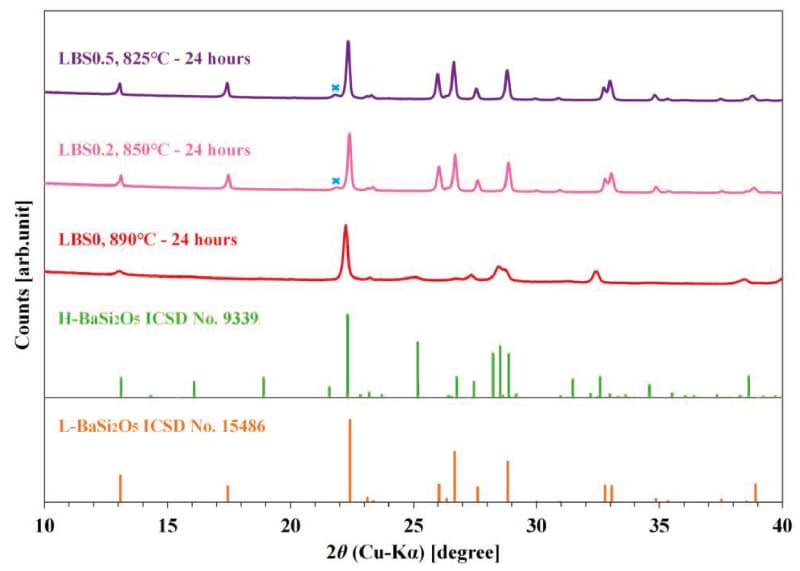 Fig.3 Comparison of XRD patterns in LBSx glasses heat-treated at near Tc for 24 hours(15). The diffraction patterns of L-BaSi2O5 and H-BaSi2O5 are shown as references. The cross mark in the figure indicates diffraction peak that is thought to be cristobalite(ICSD No. 75300).
Fig.3 Comparison of XRD patterns in LBSx glasses heat-treated at near Tc for 24 hours(15). The diffraction patterns of L-BaSi2O5 and H-BaSi2O5 are shown as references. The cross mark in the figure indicates diffraction peak that is thought to be cristobalite(ICSD No. 75300).3.3. 熱処理サンプルのラマン分光測定
図4にLBS0とLBS0.2について各熱処理における保持温度を5分から24時間まで変化させて作製したサンプルのラマン分光の測定結果(15)を示す。図4(a)より、LBS0を890℃で5分から6時間熱処理して得られたサンプルのラマンスペクトルはその形状が類似していることが分かる。一方、保持時間を24時間としたサンプルのスペクトルには鋭いピークが認められ、これは図3のXRD測定結果よりH-BaSi2O5に対応したピークであることが示唆される。図中に破線で示す533cm-1と554cm-1のピークはSi-O-Si結合の曲げモードに帰属されるピークであり、533cm-1のピークはH-BaSi2O5やL-BaSi2O5の構造と関連があることが報告されている(8,18)。図中に星印で示す554cm-1のピークはその構造の詳細は明らかになっていないが、M-BaSi2O5が存在する場合に生じるピークであることが報告されている(8,18)。533cm-1のピークに対する554cm-1のピーク強度比は保持時間の増加とともに増加しており、5分の保持でM-BaSi2O5およびH-BaSi2O5が生成し、保持時間が6時間までは熱処理に伴いM-BaSi2O5の割合が増加したことを示している。
図4(b)に、LBS0.2を850℃で種々の時間保持して作製したサンプルのラマンスペクトルを示す。保持時間が5分のサンプルでは、LBS0と比較してそのピークがブロードとなっている。これはLBS0と比較して結晶相よりもガラス相の割合が高いことを示している。保持時間が20分と30分のサンプルでは、LBS0と同様にM-BaSi2O5の存在を示唆する554cm-1のピークが確認できる。しかしながら、LBS0とは異なり554cm-1のピーク強度は533cm-1のピークよりも小さくM-BaSi2O5の生成量が少ないことを示している。また、LBS0と異なり1時間以上の熱処理ではLBS0ではみられなかったスペクトル形状となっており、これは図3の24時間保持サンプルのX R D測定結果からL-BaSi2O5に対応するスペクトルであることが示唆される。
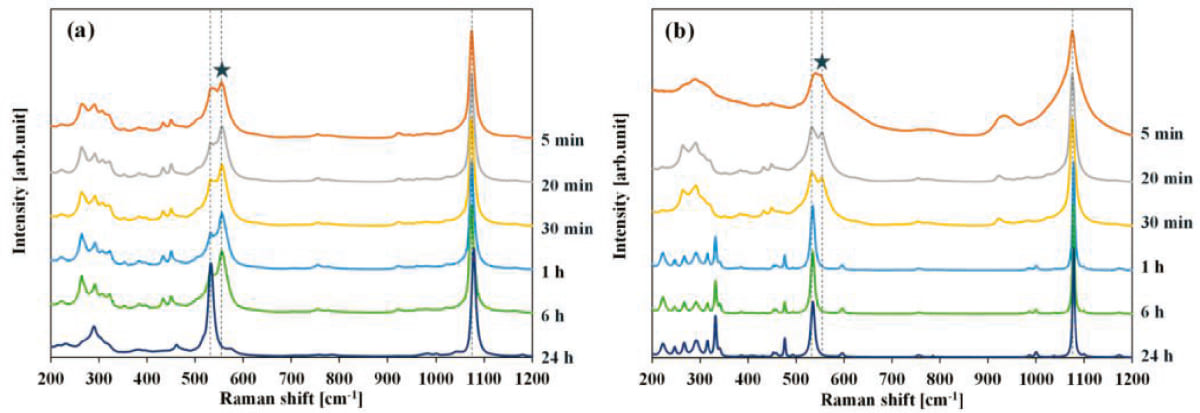 Fig.4 Raman spectra of LBS0 and LBS0.2 heat-treated at near Tc from 5 minutes to 24 hours(15). (a)LBS0 heat-treated at 890℃. (b)LBS0.2 heat-treated at 850℃. The peaks indicated by stars are metastable H-BaSi2O5 peaks seen in the early stage of crystallization of BS2 glass(8,18).
Fig.4 Raman spectra of LBS0 and LBS0.2 heat-treated at near Tc from 5 minutes to 24 hours(15). (a)LBS0 heat-treated at 890℃. (b)LBS0.2 heat-treated at 850℃. The peaks indicated by stars are metastable H-BaSi2O5 peaks seen in the early stage of crystallization of BS2 glass(8,18).3.4. 熱処理サンプルの走査透過電子顕微鏡観察
図5にLBS0の890℃ – 5分保持サンプルのSTEM観察結果(15)を示す。図5(a)のHAADF-STEM像から、高輝度の領域が低輝度領域に囲まれて存在していることが分かる。HAADF-STEM像はZコントラスト像(24)という組成の違いを反映した像であり、高輝度領域は原子番号の大きな成分で構成された領域である。図5(b)は図5(a)とは異なる領域のHAADF-STEM像であり、図5(c)は図5(b)中の四角で囲まれた領域について透過波を除く回折波のみで構成された仮想暗視野像である。この暗視野像より、低輝度領域中に10 ~ 30nm程度の高輝度領域が複数存在していることがわかる。図5(c)中の領域1と領域2の電子回折パターン(図5(d)、(e))より領域1ではガラス相の存在を示すハローパターンが確認でき、領域2では結晶相の存在を示す電子回折スポットが確認できる。
 Fig.5 STEM observation results of LBS0 heat-treated at 890℃ for 5 minutes(15).(a) HAADF-STEM image.(b)HAADF-STEM image of a region different from Fig.5(a).(c) Virtual dark-field STEM image of the area circled by the square in Fig.5(b).(d) Electron diffraction image of the region 1 in Fig.5(c).(e)Electron diffraction image of the region 2 in Fig.5(c).
Fig.5 STEM observation results of LBS0 heat-treated at 890℃ for 5 minutes(15).(a) HAADF-STEM image.(b)HAADF-STEM image of a region different from Fig.5(a).(c) Virtual dark-field STEM image of the area circled by the square in Fig.5(b).(d) Electron diffraction image of the region 1 in Fig.5(c).(e)Electron diffraction image of the region 2 in Fig.5(c).図6にLBS0.2の850℃ – 5分保持サンプルのSTEM観察結果(15)を示す。図6(a)のHAADF-STEM像から10 ~ 20nmのサイズの球状の低輝度領域が高輝度領域の中に分散していることが分かる。図6(b)のHAADF-STEM像中の領域1から領域3の電子回折パターンを図6(c) ~ 図6(e)に示す。これより低輝度領域である領域1はハローパターンが確認できることからガラス相であることが分かる。高輝度領域である領域2と領域3ではハローパターンと電子回折スポットが確認できることからガラス相の領域と結晶相の領域が混在していると言える。領域1のような球状のガラス相の存在は、熱処理によってマトリックス相とドロップレット相が生成するバイノーダル型の分相が生じたことを示している。また、領域3のような結晶相の存在は、分相後に一部の領域が結晶化したことを示唆している。
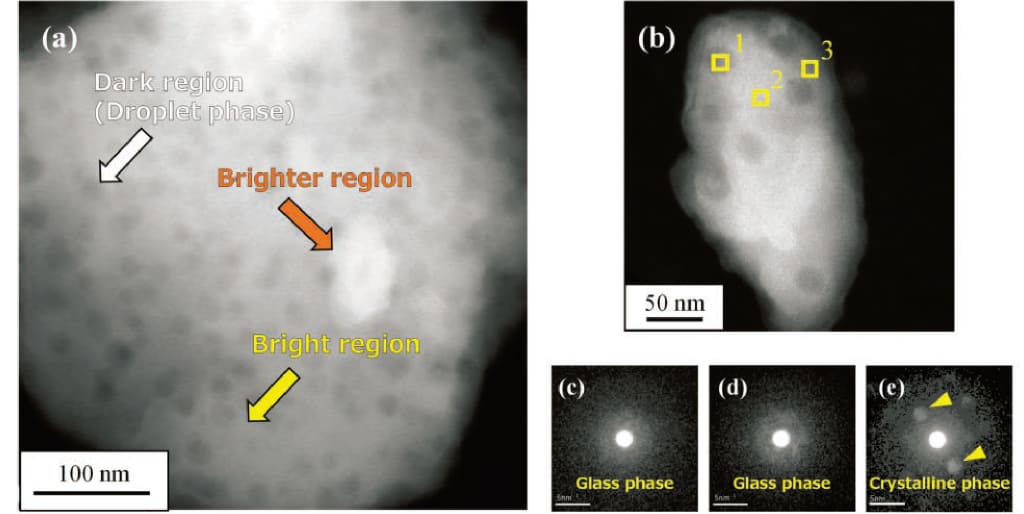 Fig.6 STEM observation results of LBS0.2 heat-treated at 850℃ for 5 minutes(15). (a)HAADF-STEM image.(b)HAADF-STEM image of a region different from Fig. 6(a).(c)Electron diffraction image of the region 1 in Fig.6(b).(d)ED image of the region 2 in Fig.6(b).(e)Electron diffraction image of the region 3 in Fig.6(b).
Fig.6 STEM observation results of LBS0.2 heat-treated at 850℃ for 5 minutes(15). (a)HAADF-STEM image.(b)HAADF-STEM image of a region different from Fig. 6(a).(c)Electron diffraction image of the region 1 in Fig.6(b).(d)ED image of the region 2 in Fig.6(b).(e)Electron diffraction image of the region 3 in Fig.6(b).図7にLBS0.5の825℃ – 5分保持サンプルのHADDF-STEM像とEDS分析結果(15)を示す。図7(a)のHAADF-STEM像よりLBS0.2と同様に低輝度のドロップレット相が確認できることからLBS0.5においてもバイノーダル分相が生じている。図7(b)はHAADF-STEM像中の低輝度領域のドロップレット相を含むようにEDSによる線分析を行った結果である。これより低輝度のドロップレット相では高輝度領域と比較してシリコンの濃度が高く、バリウムの濃度が低い組成となっていることが分かる。
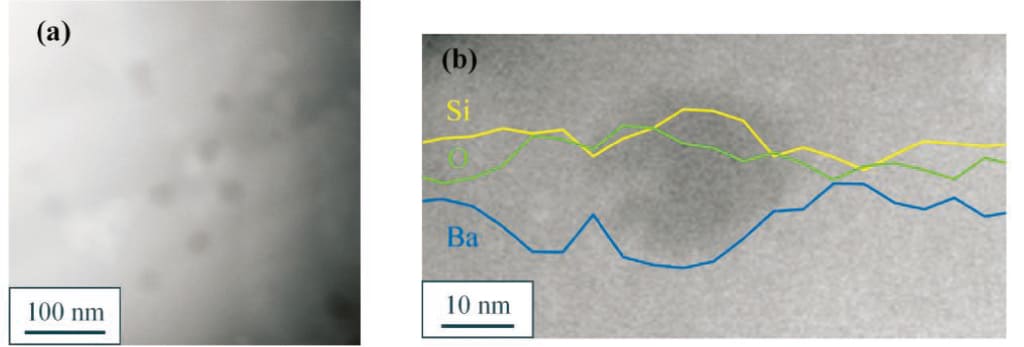 Fig.7 HAADF-STEM image and EDS line analysis of LBS0.5 heat-treated at 825℃ for 5 minutes(15).(a)HAADF-STEM image.(b)EDS line analysis result. The yellow line in the Fig.7(b)indicates Si, the blue line indicates Ba, and the green line indicates O. Li was not performed because it cannot be analyzed by EDS.
Fig.7 HAADF-STEM image and EDS line analysis of LBS0.5 heat-treated at 825℃ for 5 minutes(15).(a)HAADF-STEM image.(b)EDS line analysis result. The yellow line in the Fig.7(b)indicates Si, the blue line indicates Ba, and the green line indicates O. Li was not performed because it cannot be analyzed by EDS.4. 考察
熱処理前のガラスのDSC測定の結果(図1)、酸化リチウムの添加によってTg、T0、Tcは低温側にシフトしていた。これはHard and Soft Acids and Bases(HSAB)則(25)に基づき考察できる。Li+イオンはBa2+イオンよりもハードな酸であり、Li+イオンはBa2+イオンよりも酸素を引き付ける力が強いと考えられる。そのため、図8に示すようにガラス中のネットワークを形成しているSiO4四面体においてLi+イオンと結合している非架橋酸素がLi+イオン側にひきつけられ、Si-Oの結合力が低下し、ガラスの粘性が低下することが予想される。そのために、酸化リチウムの添加によってTg、T0、Tcは低温側にシフトしたと考えられる。一方で、LBS0.2とLBS0.5のT0 - TgはLBS0に比べて大きかったが、Tc - T0は小さかった。これよりLBS0.2とLBS0.5はLBS0と比較してガラス構造は安定だが、一旦結晶化が始まるとTcに関連する結晶相はLBS0よりも生成しやすいと考えられる。
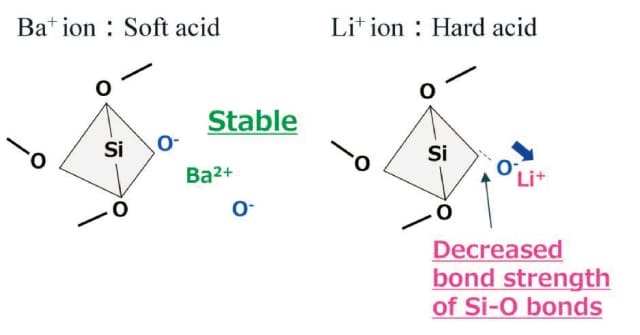 Fig.8 Image diagram of the binding force of Li+ or Ba2+ ions to non-bridged oxygen in SiO4 tetrahedra based on the HSAB rule.
Fig.8 Image diagram of the binding force of Li+ or Ba2+ ions to non-bridged oxygen in SiO4 tetrahedra based on the HSAB rule.熱処理後のサンプルのXRD測定とラマン分光測定から、LBS0とLBS0.2ではH-BaSi2O5の準安定相であるM-BaSi2O5の生成が結晶化初期において確認された(図2および4)。また、LBS0では890℃ – 5分の保持でM-BaSi2O5が生成し、保持時間の増加に伴いLBS0に含まれるM-BaSi2O5は増加し、6時間と長時間の保持でもこの構造は残存したままであった。酸化リチウムを添加したLBS0.2とLBS0.5ではそれぞれ850℃、825℃とLBS0よりも熱処理温度が低いものの、1時間以内の熱処理で、LBS0では認められなかったH-BaSi2O5からL-BaSi2O5への相変態が生じていた。
熱処理後のサンプルのSTEM観察からLBS0.2とLBS0.5では熱処理に伴いバイノーダル分相が生じ、シリコンリッチなドロップレット相とバリウムリッチなマトリックス相が生成していた(図6および7)。すなわち、マトリックス相ではシリコンの濃度が低下しバリウムの濃度が高くなるために、BaSi2O5の化学量論組成である33.3BaO-66.7SiO2[mol%]に近づくことになる。一方で、バイノーダル分相が確認されなかったLBS0では、その組成が30BaO-70SiO2[mol%]であるため、BaSi2O5の化学量論組成よりもバリウム濃度が低く、シリコン濃度が高い状態で結晶化が生じる。そのため、結晶化初期過程で生成する結晶相はバリウム量が少ない不安定な構造となる可能性がある。ガラス中のBa2+イオンの拡散速度は、ナトリウムシリケートガラスやアルカリアルミノシリケートガラスにおける他のアルカリ金属イオンやアルカリ土類金属イオンの拡散速度に比べて非常に小さいという報告(26,27)がある。このBa2+イオンの拡散速度が原因でLBS0では熱処理中にBa2+イオンの拡散が進まず、その結果として準安定構造をもったM-BaSi2O5の生成量が多くなり、24時間と長時間の熱処理でもH-BaSi2O5からL-BaSi2O5への相変態は生じなかったものと考えられる。
5. 結言
BaSi2O5の化学量論組成(33.3BaO - 66.7SiO2[mol%])よりも酸化バリウム量が少なく二酸化ケイ素量が多い30BaO-70SiO2[mol%]ガラスに少量の酸化リチウムを添加したガラスの結晶化挙動を調べ、以下の結論を得た。
- 酸化バリウムを酸化リチウムに置き換えることにより、Tg、T0、Tcが低下した。また、Tc近傍の熱処理によりH-BaSi2O5の準安定相(M-BaSi2O5)、H-BaSi2O5、L-BaSi2O5の生成が確認された。
- 酸化リチウム無添加のLBS0では、長時間の熱処理でも熱処理初期に生成したM-BaSi2O5が残存していた。
- 酸化リチウムを添加したLBS0.2とLBS0.5では、M-BaSi2O5からH-BaSi2O5への相変態と、H-BaSi2O5からL-BaSi2O5への相変態がLBS0よりもはるかに早く起こる。これは熱処理の初期段階で相分離が起こり、シリコンリッチなドロップレット相とバリウムリッチなマトリックス相が生成し、マトリックス相はBaSi2O5の化学量論組成に近い組成となることで結晶化が促進したためと考えられる。
謝辞
本研究ならびに関連論文の作成に際し、多大なご指導を賜った九州大学大学院総合理工学研究院の波多聰教授と藤野茂教授、実験データ取得に際してご尽力いただいた九州大学超顕微解析研究センターの高紅叶学術研究員と九州大学大学院総合理工学府の満田彩欄氏に、ここに謝意を表す。
参考文献
- W. Höland and G.H. Beall, 'Glass-Ceramic Technology, Third Edition'. Wiley Online Library(2019).
- E. G. Rowlands, Ph D.Thesis, University of Sheffield, (1976).
- E. G. Rowlands and P. F. James, Proc. Int. Congr. Glass, Volume 2 Extended abstracts,(2001):68-69.
- M. H. Lewis and G. Smith, J. Mater. Sci., 11[11],(1976): 2015-2026. https://doi.org/10.1007/BF02403349.
- R. M. Douglass, Am. Mineral., 43,(1958): 517-536.
- K.-F. Hesse and F. Liebau, Zeitschrift Für Kristallographie, 153,(1980): 33-41. https://doi.org/10.1524/zkri.1980.0004.
- R. S. Roth and E. M. Levin, J. Res. Natl. Bur. Stand., 62[5], (1959): 193-200.
- B. J. A. Moulton et al., CrystEngComm, 21 [17],(2019): 2768-2778. https://doi.org/10.1039/C8CE02054J.
- A. H. Ramsden and P. F. James, J. Mater. Sci., 19[5], (1984): 1406-1419. https://doi.org/10.1007/BF00563035.
- E. D. Zanotto and P. F. James, J. Non-Cryst. Solids., 104[1], (1988): 70-72. https://doi.org/10.1016/0022-3093(88) 90183-4.
- 中川英昭, 市原祥次, 熱測定, 7[1],(1980)11-17. https://doi.org/10.11311/jscta1974.7.11.
- J. D. Hanawalt, Powder Diffraction, 1[1],(1986): 7-13. https://doi.org/10.1017/S0885715600011209.
- C. Ophus, Microsc. Microanal., 25[3],(2019): 563-582. https://doi.org/10.1017/S1431927619000497.
- 梶原貴人, 博士論文, 九州大学,(2023). https://hdl.handle.net/2324/7165097.
- T. Kajihara et al., J. Am. Ceram. Soc., 106[7],(2023): 4181-4191. https://doi.org/10.1111/jace.19099.
- K.-F. Hesse and F. Liebau, Zeitschrift Für Kristallographie, 153,(1980): 3-17. https://doi.org/10.1524/zkri.1980.0002.
- M. Czank and P. R. Buseck, Zeitschrift Für Kristallographie,153,(1980): 19-32. https://doi.org/10.1524/zkri.1980.153.14.19.
- B. J. A. Moulton et al., Ceram. Int., 49[7],(2023): 10852-10863. https://doi.org/10.1016/j.ceramint.2022.11.277.
- G. Oehlschlegel, J. Am. Ceram. Soc., 58[3-4],(1975): 148. https://doi.org/10.1111/j.1151-2916.1975.tb19584.x.
- Y. Takahashi et al., Appl. Phys. Lett., 95[7],(2009):071904. https://doi.org/10.1063/1.3206931.
- Y. Takahashi et al., J. Appl. Phys., 108[6],(2010): 063507. https://doi.org/10.1063/1.3487473.
- L. Cai et al., J. Non-Cryst. Solids., 548[C],(2020): 120330. https://doi.org/10.1016/j.jnoncrysol.2020.120330.
- M. E. Mckenzie et al., Sci. Rep., 11[1],(2021): 1-15. https://doi.org/10.1038/s41598-020-79749-2.
- K. Saitoh, J. Crystallographic Soc. Jpn., 47,(2005): 9-14. https://doi.org/10.5940/jcrsj.47.9.
- R. G. Pearson, J. Am. Chem. Soc., 85[22],(1963): 3533–3539. https://doi.org/10.1021/ja00905a001.
- 寺井良平ら, 窯業協会誌, 77[3],(1969): 88-95. https://doi.org/10.2109/jcersj1950.77.883_88.
- A. Atila et al., Phys. Chem. Chem. Phys., 22, 17205-17212(2020). https://doi.org/10.1039/D0CP02910F.