2026年02月19日その他リリース
AGC Biologics社、ブラジル国家衛生監督庁よりGMP認証を取得
―シアトル拠点製造品を南米最大市場へ供給可能に―
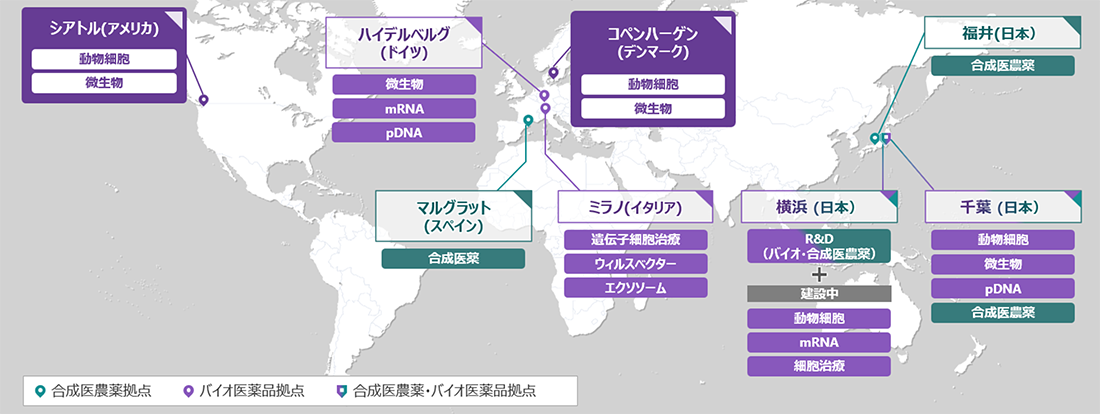
AnvisaによるGMP認証の取得は、AGC Biologics A/S(本社:デンマーク コペンハーゲン)に続き、AGCグループとして2拠点目となります*3。グローバルで統合された品質システムと拠点間の緊密な技術連携を基盤に、今後もグループ横断の供給体制をさらに拡充してまいります。

AGC Biologics社 シアトル拠点
シアトル拠点は、動物細胞・微生物由来のバイオ医薬品において、30年以上にわたる開発・製造実績を有しています。2025年には、お客様監査を含むすべての外部監査に合格するとともに、全製造ロットが品質基準を満たすバッチ成功率100%を達成するなど、品質の向上を追求しています。今回の認証取得により、同拠点が規制当局の承認を受けた国は11か国以上となりました。
AGCグループは、中期経営計画 AGC plus-2026 で3つの社会的価値を掲げています。このうち “Well-being” では、生活や医療に必要な製品・サービスを安定的に提供し、安心・安全で健康な暮らしに貢献することを目指しています。ライフサイエンス事業は、医農薬CDMOサービスを通じてグローバルで高水準の品質・サービスを提供し、各拠点のシナジーを最大化することで、社会に貢献していきます。
〈注釈〉
|
*1 |
CDMO:Contract Development and Manufacturing Organization(医薬品受託開発・製造機関) |
|
*2 |
GMP:医薬品及び医薬部外品の製造管理及び品質管理の基準 (Good Manufacturing Practice) |
|
*3 |
Anvisa取得拠点:以下地図をご参照ください。 |
■ AGC Biologics社シアトル拠点概要
|
所在地 |
米国 ワシントン州 シアトル |
|
主な対応モダリティ |
動物細胞(Mammalian)、微生物(Microbial) |
|
生産スケール・設備タイプ |
【動物細胞】 |
- ◎本件に関するお問い合わせ先:
- AGC株式会社 広報・IR部