AGC Research Report 73(2023)
Chemical valence speciation analyses of multivalent elements in glass(2)Speciation of tin ions in oxide glass containing iron oxide
ガラス中の多価元素の価数別化学分析方法の開発(2)酸化鉄を含むガラス中のスズの価数分析
西條佳孝*
Yoshitaka Saijo
*AGC株式会社 先端基盤研究所(yoshitaka.saijo@agc.com)
ガラスに添加される多価元素は、その総濃度だけではなく、価数別の濃度がガラスの特性に影響を与える。したがって、所望のガラス特性を達成するためにはガラス中多価元素の各価数の濃度を調整することが必要であり、それに伴って多価元素の価数別の濃度を定量する信頼性の高い方法が必要となる。また、それらの方法は実際の製造現場でガラスの特性を最適化するために、大量生産の現場で実行できる必要がある。ここでは、酸化鉄を含有するガラス中の価数別のスズを、一般的に使用されている装置で定量する新しい化学分析方法を開発し、検証した。ガラスを酸分解する際に、Fe3+に対する還元剤であるアスコルビン酸を添加することでFe3+を速やかにFe2+に還元し、Fe3+とSn2+の酸化還元反応を防いだうえで、液相中のSn2+をN, N-ジエチルジチオカルバミン酸ジエチルアンモニウムを溶解した有機相に抽出した。Total Sn濃度および液相に残留したSn4+濃度を ICP発光分光法にて定量し、Sn2+濃度を算出した。本方法で算出したSn2+/Total Snで定義される Sn redoxは、メスバウアー分光法で得られた値とよく一致した。さらにその方法とステップエッチング法を組み合わせることで、フロートガラスTin面からの深さ方向のtotal Sn、Sn4+、Sn2+、およびSn redoxの定量的な濃度プロファイルを得た。その結果は、先行研究の結果を支持すると共に、本方法が既存の方法よりも優れた深さ分解能を持ち、定量的な深さ方向のSnの価数別の分析方法であることを示した。
Multivalent elements are incorporated as trace elements into glass to modify its properties. Both the total concentration of multivalent elements and the specific concentration of each valency of the element significantly influence the characteristics of the glass. Therefore, accurately determining the concentration of each valency of multivalent elements in glass is crucial for optimizing its properties. Reliable methods are needed to accomplish this task, which should ideally be feasible at mass-production sites to perfect the properties of the final product. These methods should also be easily implementable using standard laboratory equipment and instruments. In this paper, we introduce and demonstrate a novel method for determining the concentrations of Sn2+ and Sn4+ in glass containing iron oxide. Ascorbic acid, acting as a reductant for Fe3+, was added during the acid decomposition of the glass samples. This was followed by the separation of Sn2+ from the decomposed solution into the organic phase as a diethyldithiocarbamate complex. We then employed inductively coupled plasma atomic emission spectroscopy to measure the concentrations of Sn4+ and total Sn, which allowed us to calculate the concentration of Sn2+. The results were confirmed by comparing the ratios of Sn2+ to total Sn(Sn redox)with results obtained from Mössbauer spectroscopy. Moreover, by integrating this method with the step etching method, we obtained quantitative concentration profiles of total Sn, Sn4+, Sn2+, and Sn redox, measured depth-wise from the tin surface of float glass. Our findings corroborate previous research and reveal that our method offers the finest depth resolution compared to existing methods.
1. 緒言
1.1. ガラス中の多価元素の役割
ガラスは幅広い組成、物性を持ち、様々-な産業分野で使用される汎用性の高い材料である。また、新たな用途に向けて、日々新しいガラス組成が開発されている。ガラスは、その主成分に加えて、微量成分が透明度[1]、色[2]、フォトルミネッセンス[3]、結晶化[4]、そして製造特性[5–7]など様々な特性に影響を与える。ガラスに添加される微量成分として多価元素が添加されることがある。また、大量生産時には、原材料や製造工程で使用する材料由来の不純物として、複数の多価元素が意図せずガラスに混入することもある。これらの多価元素は上記のガラス特性に影響し、さらに特性への影響は各価数によって異なる。したがって、実際のガラス製造において所望のガラス特性を達成するためには、ガラス中の多価元素の価数別の濃度を調整する必要がある。そのためには、多価元素の価数別の濃度を信頼性の高い方法で定量する必要がある。その定量方法には、原子価選択性、定量性、また添加される多価元素の濃度が低いため高感度が必要とされる。さらに、実際の製造現場でガラスの特性を最適化するために、これらの方法は大量生産の現場で実行できる必要がある。よって実験室で一般的に使用される機器と装置を使用して日常的に実行できる、ガラス中多価元素の価数別の濃度の定量方法が求められる。
1.2. 酸化鉄を含むガラス中のスズの価数分析[8]
多価元素の一つであるスズは、金および銅のルビーガラスの色調整剤[9]、蛍光剤[10]、および清澄剤[11,12]としてガラスに微量添加される。これらの特性発現のメカニズムには、スズの酸化還元反応がかかわっている。したがってガラス中のSn2+とSn4+の濃度を決定することは重要であり、そのための信頼できる方法が必要となる。ガラス中のSnの価数を決定する方法は、通常、化学分析と物理分析に分けられる。
化学分析の例としては、滴定[13]や分光光度法[14]がある。これらの方法は実験室で日常的に行うことができる。また、化学分析の一般的な利点は、精度が高く、検出限界が低く、コストが低いことである[15]。一方で、化学分析によりガラス中の多価元素の価数分析を行う際の一般的な問題点は、フッ化水素酸を使用した分解中に目的元素の価数が変化する可能性があることである。一般に、ガラス試料分解中の空気による酸化は、不活性雰囲気下で分解することで防ぐことが可能である[16–18]。その他に、目的元素とは異なる他の多価元素との酸化還元反応によって、目的元素の価数の変化が引き起こされる可能性がある。目的元素とは異なる他の多価元素の例としてFeが挙げられる。一般に工業用ガラスには原料として酸化鉄が意図的に添加される。また、光学特性を満足するためにできる限りFe量を下げたい場合でも、Feは他の原料に避けられない不純物として含有される[1,19]。ガラス中のFeは、ガラス分解時にイオンとして溶解し、下記に示す酸化還元電位の関係より、Snとの酸化還元反応を引き起こす(式(1)~式(3))。
しかし、以前に報告された研究[13,14]の方法では、この溶液中での酸化還元反応が考慮されていない[13]、もしくは実験室で合成された鉄を含まないガラス試料が使用されていた[14]ため溶液中での酸化還元反応については対応していない。
物理分析の例としては、メスバウアー分光法[20–24]、X線吸収微細構造(X-ray Absorption Fine Structure: XAFS)[25–27]、高分解能型波長分散型蛍光X線分光分析(High Resolution X-ray Fluorescence : HR- XR F)[28,2 9]、およびX線光電子分光 法(X-ray Photoelectron Spectroscopy : XPS)[30]がある。これらの物理分析の一般的な利点は、元素選択性が高いことである。一方でいくつかの欠点もある。XAFSは放射光施設の使用を必要とし、日常的な使用はできない。HR-XRFは、二結晶型の機構のため、S/N比が低い。十分なS/N比を得るためには長時間の分析が必要となる。XPSはその分析深さが10nm未満であり、ガラス試料のバルクのSn価数を決定するには浅すぎる。また通常、正確に価数を決定するためには1mass%以上のSnが含有される必要があり、微量しか添加されない場合には適用が困難である。
このように、化学分析と物理分析のどちらにも長所と短所があるが、実験室で一般的に使用される機器と装置を使用して日常的に実行できる方法としては、化学分析が好ましいと考えられる。さらに、前述したように、実際の工業用ガラスにはSnのみではなく、多価元素としてFeが含有される場合が多い。そのため、本研究の目的は、実験室で一般的に使用される機器と装置を使用して日常的に実行できる、Feを含むガラス中のSnの価数分析方法を確立することとする。そのための第一の課題は、ガラス分解時に式(3)に示されるSn2+とFe3+の間の酸化還元反応を防ぎ、Sn価数を維持することである。これにはいくつかの可能なアプローチが考えらえる。1, 酸化還元反応を遅くし、実質的に反応を排除する[31]、2, Fe3+をマスキングする[32]、および3, 酸化還元反応を引き起こす前に溶液中からFe3+を排除する[33]、などである。この研究では、分解溶液に還元剤を添加してFe3+を還元し、Sn2+とFe3+の間の酸化還元反応を防止することを考えた。ここでは還元剤としてアスコルビン酸 (C6H8O6)を選択した。その酸化還元電位およびFe3+との酸化還元反応をそれぞれ式(4)、式(5)に示す。アスコルビン酸とFe3+間の酸化還元反応はpH1.5以下で容易に起こり、かつSnとの酸化還元反応を起こさないことが示されている[34]。
第二の課題は、Snの各価数、すなわちSn2+とSn4+の濃度を別々に測定することである。ここでも、いくつかのアプローチが考えられる。1, いずれかのイオンを着色し、比色法を使用する[16,17]、2, 揮発分離法を用いていずれかのイオンを分離する[18]、3, 溶媒抽出法を用いて各イオンを分離する、といったアプローチである。この研究では、ジエチルジチオカルバミン酸(DDTC)を利用した溶媒抽出法を検討した。これは、pH1~2.2の範囲でSn2+が選択的かつ定量的に有機相に抽出されるためである[35][36]。本研究では上記の2点の課題に対するアプローチをSn(酸化スズ)およびFe(酸化鉄)をドープし調製したソーダライムシリケートガラス材料に適用し、メスバウアー分光法によって得られたSnの平均価数と比較することによって検証する。
1.3. フロートガラスに侵入したスズの深さ方向の価数分析[37]
フロート法は板状のガラスを量産する技術の一つである。この方法では、N2/H2ガスを流した還元性雰囲気下で、溶融ガラスを溶融スズの上に浮かべることで板状のガラスを成形する[38]。従来のソーダライムシリケートガラス[38]に加え、ホウケイ酸ガラス[39]、フラットパネルディスプレイガラス[40]、導光板ガラス[1]、化学強化用ガラス[41]などの高品質ガラスがこの製法で製造されている。溶融スズは、溶融スズと接するガラス面(本報告ではTin面と呼称する)に侵入することが知られており[42]、Tin面はガラスの溶融スズと接しない面(本報告ではAir面と呼称する)とは異なる性質を示す[43–48]。高品質なガラス表面を実現するためには、ガラスTin面と溶融スズの間の反応を詳細に理解する必要がある。先行研究においては、Tin面に侵入したスズがガラス内の多価元素と反応することで、ガラス深さ方向に複雑なSn濃度プロファイルおよび酸化還元プロファイルを示すことが明らかになっている[26,42,49–51]。これらのプロファイルは、下記に示す拡散-反応モデルにて説明されている[44,46,49–52]。
a)溶融ガラスがフロートバスに入る際、溶融スズを通過した雰囲気中の水素がガラスTin面に侵入し[49]、Tin面表層のFe3+およびS6+がFe2+およびS2-に還元される。これにより、Tin面の表面にはFe3+やS6+を含まない還元層が形成される。ガラスに侵入可能なSn2+は2つの方法で生成されると言われている。一つはフロートバス内の少量の残留酸素により溶融スズ(Sn0)が酸化されること[49]、もう一つは溶融スズ(Sn0)とガラスTin面表面のFe3+やS6+との酸化還元反応により溶融スズ(Sn0)が酸化されることである[46,51]。生成したこれらのSn2+は、2つのNa+、またはFe2+とのイオン交換反応により、Tin面の表層に侵入する。b)Tin面の表層に侵入したSn2+は、ガラスメルト内部でのイオン交換反応により、ガラス内部に拡散する[46,49,50,52]。したがって、Sn2+の拡散係数に従った濃度プロファイルを示す。
c)ガラスメルトに拡散したSn2+は、ガラスメルト深部でFe3+[26,49–53]もしくはS6+[26]との酸化還元反応によってSn4+に酸化される。生成したSn4+は、その拡散係数に従って拡散する。Sn4+の拡散係数は、Sn2+の拡散係数よりも小さい[44]。これらの結果、還元層内では、Sn4+が存在せず、Sn2+の拡散係数に従った濃度プロファイルを示すが、より深い領域では、Sn4+の拡散係数に対応する濃度プロファイルを示す。
d)Total Sn濃度プロファイルは、Sn2+およびSn4+濃度プロファイルを足し合わせたものとなる。その結果、Sn4+が生成した深さでtin humpと呼ばれるサテライトピークが生成する。Tin humpより浅い部分は還元層、tin humpより深い部分は酸化層と呼称される。
以上のようにTin面に侵入したSnはガラス内部で酸化還元反応を受けるため、Tin面表面から深さ方向の total Sn濃度プロファイルだけでなく、Sn2+、Sn4+、およびSn2+/total Snの割合で定義されるSn redoxの深さ方向プロファイルも重要である。
Tin面の深さ方向のtotal Sn濃度プロファイルの測定方法としては、EPMA[23,24,26,42,46]、XRF[23]、二次イオン質量分析法(Secondary Ion Mass Spectrometry, SIMS)[49]、XPS[23,44,54]、およびラザフォード後方散乱分光法(Rutherford Backscattering Spectrometry, RBS)[46,55]があげられる。
同様にTin面の深さ方向のSn redoxプロファイルの測定方法としては、透過型メスバウアー分光法(Transmittance Mössbauer Spectroscopy, TMS)[23,24,56]、内部変換電子メスバウアー分光法(Conversion Electron Mössbauer Spectroscopy, CEMS)[24,46,50–52,57]、放射光XAFS[26]があげられる。
ただし、深さ方向のSn redoxプロファイルを測定するこれらの方法は、定量性に欠ける、機器や設備の使用が制限される、という問題がある。メスバウアー分光法でSn redoxを定量的に決定するためにはSn2+およびSn4+イオンのデバイ温度の正確な測定が必要となる。デバイ温度を正確に決定するには、異なる温度で複数の測定を実行する必要があり、分析時間が長くなる。Williamsらの報告[24]によると、フロートガラスのTin面の最表面のSn4+のデバイ温度と、ガラス内部のSn4+のデバイ温度が異なることが指摘されている。これは深さ方向のSn redoxプロファイルを定量的に決定するためには、デバイ温度を各深さで測定する必要があることを示しており、事実上測定は不可能と言える。なおCEMSの深さ分解能は2μm程度と言われている[24,58]。XAFSに関してFlankらは[26]はガラスTin面の深さ方向の価数分析を行ったが、これは定量的ではなくSnの価数の変化のトレンドを示したのみである。また、サンプル調製に使用された接着剤のためにサンプルの最表面数μm部分は明確に分析できなかった。また放射光施設を使用する必要があるため、日常的な測定はできない。一方でXAFSを用いた方法では、深さの分解能は1μmと高い。
以上のように、これまでフロートガラスTin面のSn2+、Sn4+、およびSn redoxの深さプロファイルを定量的に測定する方法は示されていない。さらに、実際のガラス製造に活用することを考えると、実験室で一般的に使用される装置を使用してこれらを測定できることが好ましい。そのため、ここではバルクガラスに適用したスズの価数分析方法[8]と、フロートガラスのAir面表層のFe2+およびtotal Fe濃度を定量するために使用されたステップエッチング技術[17]を組み合わせた新しい方法を提案し、先行研究と比較、議論する。
2. 実験
2.1. 試料
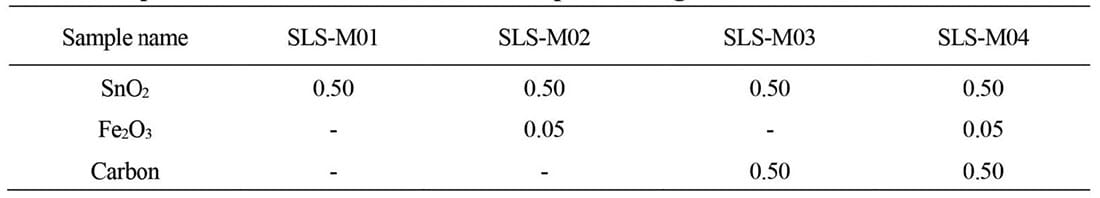
ガラスバルク中のSnの価数分析用には、16.5Na2O–9.4CaO–74.1SiO2(mass%)の母組成で、微量成分として0.5mass% SnO2、0 - 0.05mass% Fe2O3を外割で添加したソーダライムシリケートガラスを作製し分析に供した。ガラスサンプルは原料としてNa2CO3、CaCO3、およびSiO2を用い、還元剤として0 - 0.05mass%のコークス(Carbon)を添加しPtるつぼを用いて1500℃にて溶解することで得た。Table 1に、使用したサンプル名と添加濃度を示す。
深さ方向のSnの価数分析用には、AGC製の板厚3.2mmのソーダライムシリケートガラスを用いた。組成は71SiO2–13Na2O–9CaO–5MgO–2Al2O3(mass%)であり、微量添加物として0.5mass% Fe2O3および0.2mass% SO3を含有する。また密度は2.50g/cm3である。
2.2. 装置および使用機器
ガラスバルク中のSnの価数分析用には、ガラス試料の分解容器として120mLのポリテトラフルオロエチレン(PTFE)製の分解容器、分解時の攪拌のために磁気スターラーと長さ40mm × 直径7mmの撹拌子を使用した。試薬を容器に加えるために、コック付き100mLポリプロピレン(PP)製分液ロートを使用した。有機溶媒抽出のため、100mLガラス分液ロートを用いた。溶液の定容には50mLメスフラスコを用いた。分解溶液を移す際にテルモ株式会社製10mLシリンジおよび東洋濾紙株式会社製孔径0.45μmのシリンジフィルターを用いた。各元素の定量には日立ハイテク株式会社製ICP-AES SPS5520を使用した。
板状のガラスの深さ方向のSnの価数分析用には、エッチングのための超音波洗浄機としてAS ONE株式会社製VS-100IIIを用いた。ガラス試料のマスキングにはTERAO KA株式会社製ポリイミドテープ(Kapton®フィルム粘着テープ 650S #50)を使用した。
2.3. 試薬
関東化学株式会社製の原子吸光法用のフッ化水素酸(50mass%)、塩酸(36mass%)、および過塩素酸(60mass%)、鹿特級の混合キシレン、ホウ酸、およびアスコルビン酸、Sn、Si標準液(1g/L)、富士フイルム和光純薬株式会社製の和光1級のN, N-ジエチルジチオカルバミン酸ジエチルアンモニウム、AGC株式会社製のCYTOP® CTL-809Mを使用した。超純水は減圧攪拌法にて2時間以上脱気したものを用いた。
2.4. 分析方法
ガラス試料の分解およびエッチング
ガラスバルク中のSnの価数分析に関しては、ガラス試料をメノウ乳鉢とメノウ乳棒で粉砕した。粉砕した試料を電気乾燥機にて110℃で2時間乾燥した。Fig.1にバルク状のガラスサンプルの分解に使用される装置の概略を示す。粉砕および乾燥したガラス試料 30mgをPTFE分解容器に添加し、5mass% アスコルビン酸1mLを加えた。12mol/L HF 4mLおよび6mol/L HCl 10mLを分解容器に接続されたPP製分液ロートに加えた。分解容器内の酸素を追い出すために、窒素ガスを約10mL/sで5分間通じた。ロート内のHF-HCl溶液を分解容器に加えた後、窒素ガスを約10mL/sで通じながら、30分間攪拌することにより、ガラス試料を分解した。分解中にPP製分液ロートに4mass%のホウ酸溶液10mLを追加した。分解が終了した後、ホウ酸溶液を分解容器に加え、1分間攪拌した。ホウ酸は、HFをマスキングするため添加した[59]。なお、その溶液は実質的にガラス器具を侵さない[60,61]。PTFE分解容器を開け、容器内の溶液を50mLメスフラスコに移した。容器を洗浄するために少量の超純水を加え、その超純水を同じ50mLメスフラスコに移し、さらに超純水で50mL定容した。本溶液にはガラス試料に含まれていたtotal Snが含有されるため、バルクtotal Sn溶液と呼称する。
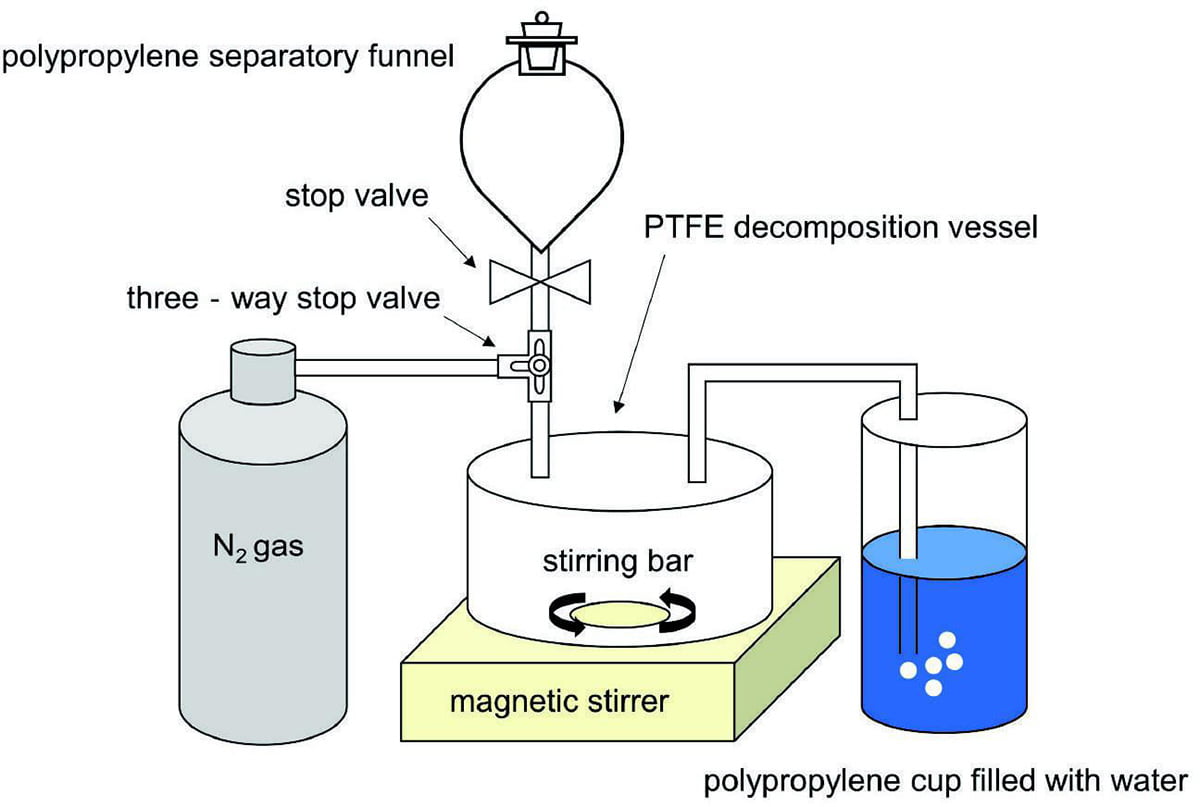 Fig.1 Schematic representation of the experimental setup for decomposition of the glass samples. Glass samples are decomposed in the PTFE decomposition vessel with nitrogen flow. The nitrogen flow in the vessel is confirmed by the presence of nitrogen bubbles in a polypropylene cup filled with water.
Fig.1 Schematic representation of the experimental setup for decomposition of the glass samples. Glass samples are decomposed in the PTFE decomposition vessel with nitrogen flow. The nitrogen flow in the vessel is confirmed by the presence of nitrogen bubbles in a polypropylene cup filled with water.板状ガラスの深さ方向のSn価数分析に関しては、まずガラスカッターを用いて試料を4cm x 4cmの大きさの小片に切断し、分析面であるTin面にカプトンテープを貼付した。カプトンテープ貼付面以外の全ての面にCYTOP®を塗布し、焼成(50℃ x 1h → 80℃ x 1h → 150℃ x 1h)し、冷却した後にカプトンテープを除去した。試料をポリエチレン袋に入れ、5mass%アスコルビン酸1mLと、1.4mol/L HFおよび0.12mol/L HClの混合液10mLを加えた。サンプルとエッチング液を含むポリエチレン袋を、水道水を満たしたガラス製ビーカーに入れた。Sn2+の酸化を防ぐために、ガラスベルに窒素ガスを通じ、不活性雰囲気を保った。エッチングに使用される実験装置の概略図をFig.2に示す。本エッチングは、必要なエッチング深さに応じて、28 kHzで超音波を印加しながら、2~4分間行った。なお必要なエッチング時間は事前にエッチングレートを調査したうえで決定した。所定の時間のエッチングが終了した後、エッチング液を30mLポリプロピレンカップに移した。4mass%ホウ酸5mLを試料が含まれるポリエチレン袋に加え、試料を洗浄した後に同じ30mLポリプロピレンカップに加えた。この操作はSn2+の空気酸化を防ぐため素早く行い、2回繰り返した。その後、超純水にて同様に試料を洗浄した後、30mLに定容した。本溶液にはガラス試料に含まれていたtotal Snが含有されるため、表面total Sn溶液と呼称する。
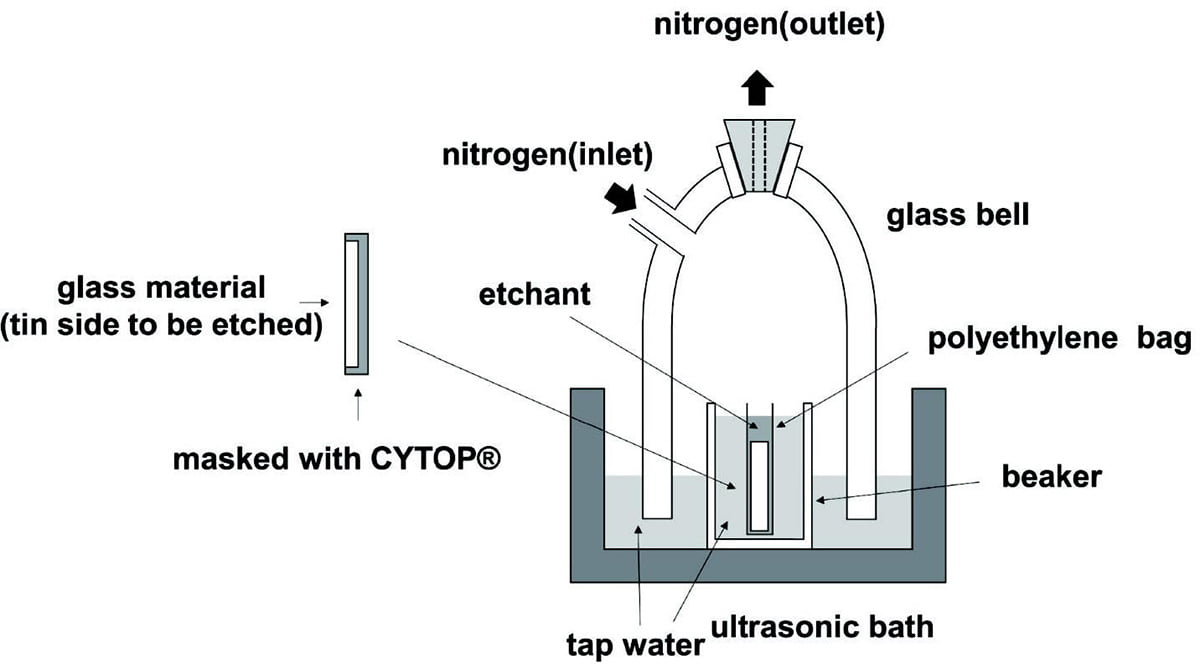 Fig.2 Schematic representation of the experimental setup for etching of the glass sample. The sample is etched in the polyethylene bag with ultrasonication at 28 kHz under nitrogen flow.
Fig.2 Schematic representation of the experimental setup for etching of the glass sample. The sample is etched in the polyethylene bag with ultrasonication at 28 kHz under nitrogen flow.バルクtotal Sn溶液、表面total Sn溶液いずれについても、以下の操作にてSnの価数分離を行った。シリンジを用い約10mLを2回採取した。20mLのtotal Sn溶液を、0.1mass% DDTCキシレン溶液5mLを添加した100mLのガラス製分液ロートにシリンジフィルターを使用して添加した。素早くロートを1分間振とうし、total Sn溶液中のSn2+を有機相に抽出した。この抽出手順は新しい有機相を用い、繰り返し2回行った。その後、ロート内の下層の水相を採取した。本溶液にはガラス試料に含まれていたSn4+が含有されるため、ガラスバルク中のSnの価数分析ではバルク Sn4+溶液、板状ガラスの深さ方向のSn価数分析では表面Sn4+溶液と呼称する。なお、ガラスバルク中の Snの価数分析については、これらの分析を同じ条件で3回繰り返し行った。
SnおよびSiの定量
バルクtotal Sn溶液、表面total Sn溶液、バルク Sn4+溶液、および表面Sn4+溶液中のSn、また表面total Sn溶液中のSiをICP発光分光法にて定量した。定量の際は、溶液のマトリックス(HF、HCl、ホウ酸、および超純水)を合わせた標準溶液を用いた。ICP発光分光法の条件をTable 2に示す。Sn redoxおよび板状ガラスのエッチング深さはそれぞれ式(6)および式(7)に従って算出した。
ブランクテスト
ガラスバルク中のSnの価数分析、板状ガラスの深さ方向のSn価数分析いずれも空操作を4回繰り返し行い、空試験値の平均およびその標準偏差(σ)を算出した。定量下限値を空試験値の平均に10σを加えたものとした。
メスバウアー分光法によるSn価数分析
過去の報告[23,58,62]を参考に、板状のSLS-M01~04試料に対し、室温における119Snメスバウアースペクトルを通常の透過法にて測定した。Sn4+ サイトおよびSn2+ サイトのデバイ温度を実験的に求め、室温における無反跳分率を見積るため、4個の試料のうち SLS-M03試料に対し、液体窒素フロー型クライオスタットを用いて、測定配置を変えずに温度4点(78K, 100K, 200K, 300K)における119Snメスバウアースペクトルを通常の透過法にて測定した。線源には Ca119mSnO3を用い、線源のドップラー速度範囲は ± 8mm/s.速度校正はα-Fe箔標準試料を用いて行い、速度0mm/sの基準はCaSnO3(Sn4+)標準試料のピーク位置に設定した。線源のSnから出る妨害K-X線カット用フィルターとしてPd 50μm箔を使用した。γ線検出にはNaIシンチレーションカウンターを使用した。線源放射能は444~416MBq = 12.0~11.2mCiであった。
メスバウアースペクトルのフィッティング
酸化雰囲気にて調製したSLS-M01およびM02試料に対しては、Sn4+に対応する四極子分裂ダブレット1組とSn2+に対応する四極子分裂ダブレット1組の、ダブレット2組(ローレンツ曲線2本 × 2組)で最小二乗フィッティングした。還元雰囲気試料(SLS-M03およびM04)に対しては、Sn2+に対応するダブレットの高さの比および幅の比が1 : 1からずれていることに対応するためSn4+に対応する四極子分裂ダブレット1組とSn2+に対応する四極子分裂ダブレット2組のダブレット3組で最小二乗フィッティングした。なおSn2+のダブレット2組は、ピークが連続的に繋がっているため、一意的な分離は困難だが、トータルのSn2+の割合は分離の仕方にほとんど依存しなかった。バルクのガラス試料のため試料中に結晶方向の配向性や結晶振動の異方性はないと仮定し、何れのダブレット成分に対しても、左右2本のピークの面積強度比を1 : 1に固定し解析した。なお、Sn2+由来のピークとSn4+由来のピークを分離する際の不確かさは約2%と見積もられた。
無反跳分率の補正およびSn redoxの算出
SLS-M03試料のスペクトルの積分吸収強度の温度依存性にデバイモデルの高温近似式(8)を適用し、Sn4+サイトとSn2+サイトのデバイ温度を求めた。求めたデバイ温度を用いて、式(9)および(10)より各測定温度におけるSn4+サイトとSn2+サイトの無反跳分率を求めた。
今回のバルク試料に関しては、試料間で組成がほぼ同じであることから、SLS-M03試料に対して得られたデバイ温度がすべての試料に共通であると仮定し、各試料に対して実験的に得られた積分吸収強度に無反跳分率の補正を加えた強度比を算出し、Sn4+サイトと Sn2+サイトの原子存在比を求め、Sn redoxを算出した。
3. 結果および考察
3.1. 定量下限
ガラスバルク中のSnの価数分析において、定量下限値は、total Snについては0.003mass%(as SnO2)、Sn4+については0.004mass%(as SnO2)であった。板状ガラスの深さ方向のSn価数分析において、今回の条件(16(4 x 4)cm2)のガラスを1μm深さでエッチングしたとき、total SnおよびSn4+の定量下限値はいずれも0.02mass%(as SnO2)であった。
3.2. バルク試料中のSnの価数分析結果および考察
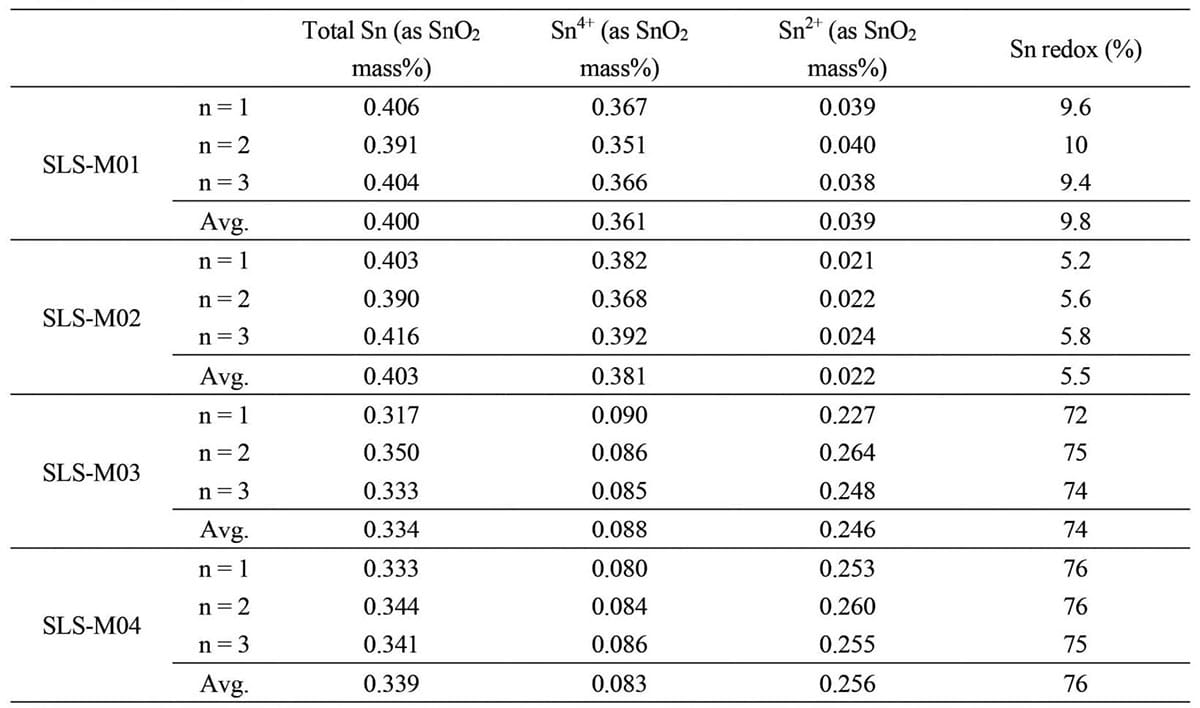
Table 3にガラスバルク試料(SLS-M01~04)のtotal Sn濃度、Sn4+濃度、Sn2+濃度(全てas SnO2mass%)、およびSn redoxの分析結果を示す。3回の繰り返し実験における再現性は良好である。還元性の雰囲気で作製したSLS-M03およびM04のSn redoxは酸化性の雰囲気で作製したSLS-M01およびM02に対して高く、作製雰囲気を反映した結果が得られている。Fig.3に室温(300K)での各サンプルのメスバウ アースペクトルを示す。SLS-M03について測定温度違い(78~300K)でのメスバウアースペクトルから求めた、SLS-M03中のSn2+およびSn4+のデバイ温度 θDはそれぞれ185K, 266Kであった[8]。これらの値は、過去のソーダライムガラス中のSn2+およびSn4+のデバイ温度の測定結果[23,56,58]によく一致した。よってSLS-M03のSn2+および Sn4+のデバイ温度を、それと組成がほぼ同じ他の試料に適用することは妥当であると判断した。またそこから算出された室温におけるSn2+およびSn4+の無反跳分率はそれぞれ0.21, 0.47であった。Table 4に無反跳分率を補正したSLS-M01~M04のSn redoxを示す。化学分析の結果と同様に SLS-M03およびM04のSn redoxはSLS-M01および M02に対して高かった。

 ここで∫は無反跳分率、Tは測定温度、θDはデバイ温度、kBはボルツマン定数、ERは反跳エネルギー、Eγはメスバウアーガンマ線エネルギー(23.87keV)、Mは反跳核質量(118.90331u)、cは光速度、Aは積分吸収強度を示す。
ここで∫は無反跳分率、Tは測定温度、θDはデバイ温度、kBはボルツマン定数、ERは反跳エネルギー、Eγはメスバウアーガンマ線エネルギー(23.87keV)、Mは反跳核質量(118.90331u)、cは光速度、Aは積分吸収強度を示す。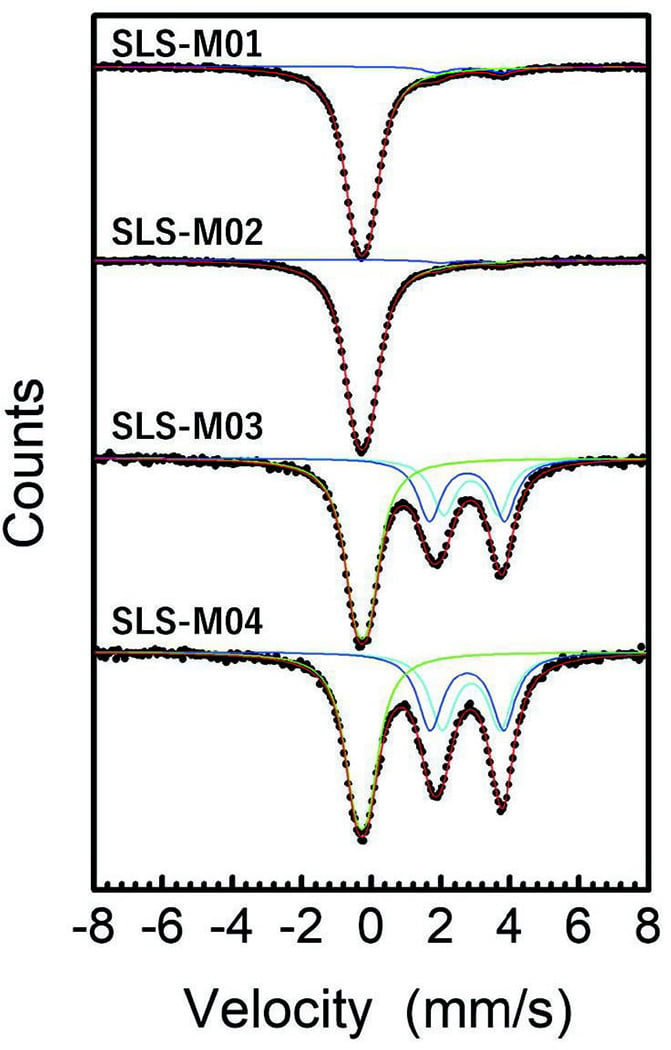 Fig.3 Mössbauer spectra of glass samples with standard soda lime silicate glassmass% composition 16.5Na2O・9.4CaO・74.1SiO2, doped with 0.5mass% SnO2 at room temperature(300K). Red line shows the fitting result of the measurement result(black circles). Green line shows the fitting result of Sn4+. Blue and light blue lines show the fitting results of Sn2+. Because the peaks of the two sets of Sn2+ doublets of SLS-M03 and SLS-M04 are connected continuously, it is difficult to deconvolute them uniquely, as discussed in the text.
Fig.3 Mössbauer spectra of glass samples with standard soda lime silicate glassmass% composition 16.5Na2O・9.4CaO・74.1SiO2, doped with 0.5mass% SnO2 at room temperature(300K). Red line shows the fitting result of the measurement result(black circles). Green line shows the fitting result of Sn4+. Blue and light blue lines show the fitting results of Sn2+. Because the peaks of the two sets of Sn2+ doublets of SLS-M03 and SLS-M04 are connected continuously, it is difficult to deconvolute them uniquely, as discussed in the text.Fig.4に二つの方法で測定されたSn redoxの比較を示す。x軸のメスバウアー分光法のエラーバーは、ピーク分離の不確かさとして2%とした。y軸の化学分析法のエラーバーは繰り返し測定の結果の1σとした。これらの二つの方法によるSn redox分析結果は、酸化鉄を含むサンプルの結果を含め、よく一致した。よって新規に提案された化学分析方法の妥当性が検証されたと考えられる。なお、その他に行った妥当性の検証の詳細は原著論文[8]を参照願う。
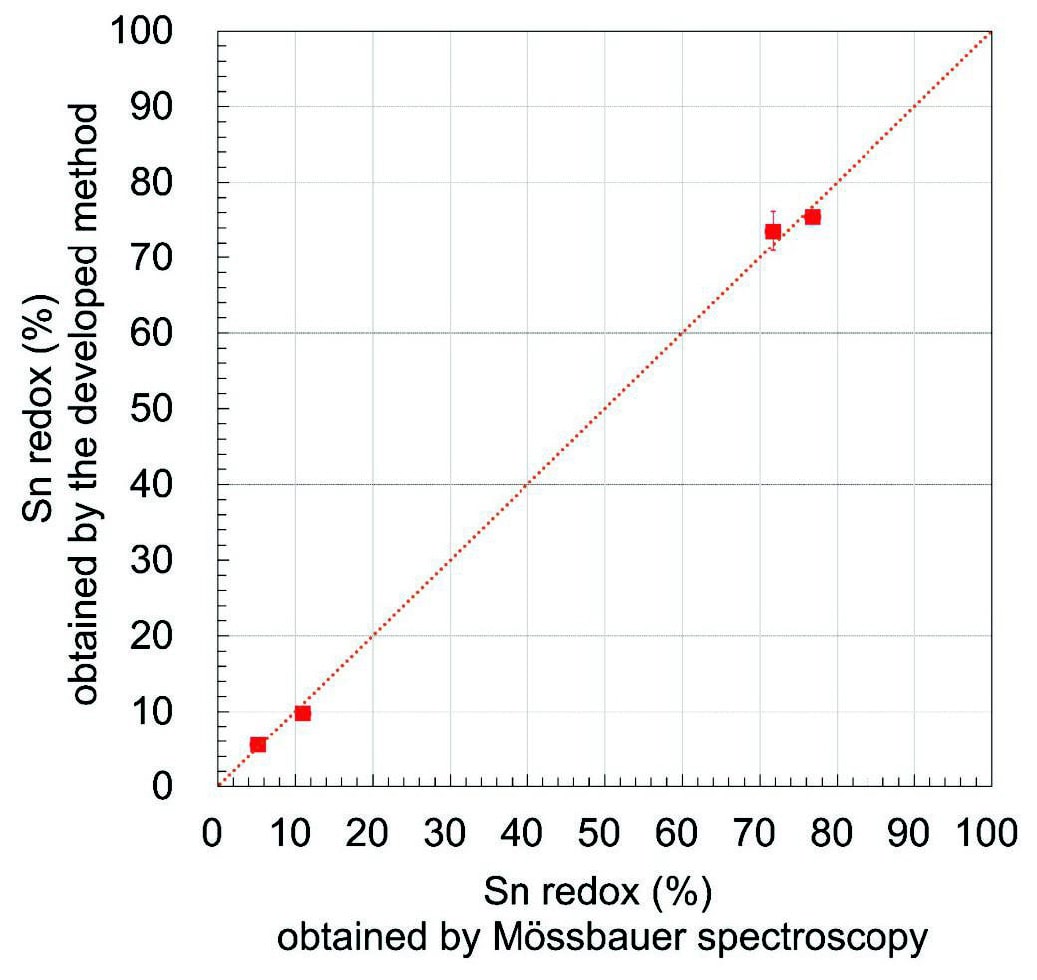 Fig.4 Comparison of the Sn redox obtained by Mössbauer spectroscopy and the proposed method. The values measured by Mössbauer spectroscopy were corrected with the recoilless fractions at room temperature(300K). The red dotted line indicates y=x for reference.
Fig.4 Comparison of the Sn redox obtained by Mössbauer spectroscopy and the proposed method. The values measured by Mössbauer spectroscopy were corrected with the recoilless fractions at room temperature(300K). The red dotted line indicates y=x for reference.3.3. 板状の試料の深さ方向のSn価数分析結果および考察
Fig.5に板ガラスのTin面から深さ方向に対する total Sn、Sn4+、Sn2+濃度、およびSn redoxを示す。Total Sn濃度は最表面で約1.4mass%であり、最表面から深さ方向に急激に減少し、7~8μm深さでピークを示した。この内部のピークはいわゆるスズのサテライトピーク(tin hump)で、その濃度は約0.6mass%であった。Total Sn 濃度はtin humpより深い部分で緩やかに減少し、深さ17μmで0.05mass%未満であった。Sn2+濃度は表面から単純に減少し、内部にピークは見られなかった。一方でSn4+濃度は複雑なプロファイルを示した。最初のピークは最も外側の表面にあり、2番目のピークは7~8μm深さにあり、tin humpの深さと一致した。これらの結果から計算されたSn redoxプロファイルは、最表面で53%の値を示し、その後、深さ1.5μmで最大値である75%まで増加し、6μmで51%まで徐々に減少し、その後7~8μm深さで 13%まで急激に減少した。この深さは、tin humpの深さと一致していた。Tin humpより深い部分では、Sn redoxは10%未満まで徐々に減少した。Tin humpより浅い部分はいわゆる還元層であり、tin humpより深い部分はいわゆる酸化層であると言える。
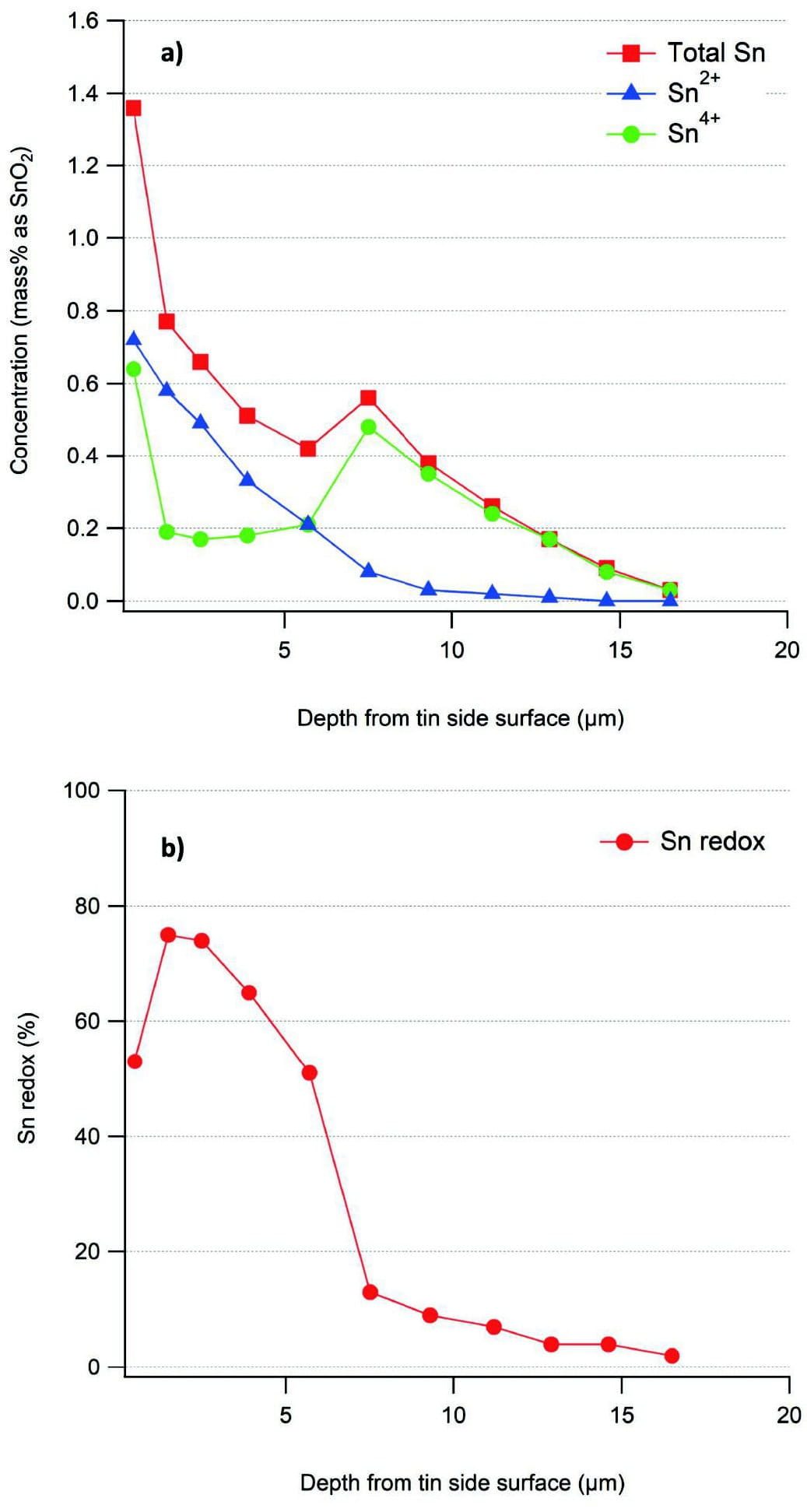 Fig.5 a)Concentration of total Sn, Sn2+, and Sn4+; b)Sn redox, as a function of depth from the tin side
Fig.5 a)Concentration of total Sn, Sn2+, and Sn4+; b)Sn redox, as a function of depth from the tin sideここで本報告にて得られた結果について考察を行う。最表面のSn4+ピークは、ガラスがフロートバスから酸化雰囲気(大気)に晒される際にSn2+が低温酸化することに起因し生成すると説明されている[24,47,52]。Total Snに対するSn2+もしくはSn4+の割合については、最表面を除くtin humpよりも浅い領域では、Sn2+が多く(Sn redoxが高く)、tin humpより深い部分では、total Snの約90%がSn4+である(Sn redoxが約10%)ことが定量的に明らかとなった。これは先行研究[23,24,26,49–52,56]の結果と定性的に一致しており、従来示された拡散および酸化還元メカニズムを支持する。
一方で、本研究では、tin humpよりも浅い還元層領域に一定量のSn4+が存在することを明らかにした。Johnsonら[23]も同じ結果を確認しているが、明確な説明はなかった。還元層領域に一定量のSn4+が存在することは、Sn2+の侵入速度が、還元雰囲気によって表面からガラス中の多価元素(主にFe3+およびS6+)が還元される速度よりも高い場合に説明できるとされている[63]。これは、最終的にtin humpが形成される深さより浅い領域に存在していたFe3+およびS6+により、侵入してきたSn2+が酸化されることによって、Sn4+が生成可能ということを示す。
本研究ではフロートガラスTin面の詳細な深さ方向 Snプロファイル(価数ごと、redox換算)を高い定量分解能と深さ分解能で明らかにしたが、フロートガラスTin面のSnプロファイルは一般に製造条件に複雑に影響を受ける。例として下記があげられる。
- ガラスの母組成
- フロートバス内の雰囲気(酸素濃度を含む、また場所ごとの違いも含む)
- ガラスの厚さ(フロートバス内の滞留時間、延伸、または圧縮効果)
- ガラス中の多価元素の種類および濃度
- 各温度でのSn2+とSn4+の拡散係数
したがって、本研究で新たにフロートガラスTin面の深さ方向SnプロファイルをSn2+とSn4+に分けて定量的な議論ができるようになったものの、フロートガラスTin面に侵入したSnのプロファイルの形成メカニズム、またフロートガラスのTin面における多種の多価元素間の酸化還元機構を完全に理解するにはまだ十分ではない。フロートガラスのTin面におけるSnプロファイル形成メカニズムおよび多種の多価元素間の酸化還元機構をより深く理解するためには、ガラスTin面の深さ方向の価数別のFeおよびSの分析方法を開発し実試料に適用し、さらにそれらの結果を用いてシミュレーションを行う必要があると考えている。これにより、tin humpよりも浅い還元層領域に一定量存在するSn4+の生成理由についても考察が可能になる。
ここで本方法について先行研究例と比較を行う。第 1章で述べたように、先行研究の方法(TMS、CEMS、およびXAFS)では実質的に深さ方向のSn価数ごとの定量化はできない。そのため、本研究にて提案された方法が既存の方法と比較して最も定量的であることは明らかである。深さ方向分解能に関しては、本方法によるエッチング深さは、エッチング時間によって変えることができる。1μm深さでエッチングしたとき、total SnおよびSn4+の定量下限値はいずれも0.02mass%(as SnO2)であるため、0.1μm深さでエッチングした際のtotal SnおよびSn4+の定量下限値はいずれも0.2mass%(as SnO2)となる。よって、total SnおよびSn4+が0.2mass%(as SnO2)以上存在する際は、エッチング量を0.1μmまで低減しても深さ方向に定量分析することが可能である。したがって本方法は先行研究例の中で深さ方向分解能が最も良いXAFS(深さ方向分解能1μm)よりも良い(小さい)深さ方向分解能を持つ。さらに、XAFSは放射光施設を利用するため実験に至るまでに時間を要すること、TMSやCEMSは分析自体に長時間を要することに対して、本方法は1サンプルあたり3日で分析可能であるため、分析にかかる時間は先行研究例と比較し有利である。また本法は一般的に使用される装置と機器のみを使用するため、一般の実験室で実行可能である。
4. 結言
酸化鉄を含むソーダライムシリケートガラス中の価数ごとのスズ濃度について一般的に使用されている装置で定量する新しい化学分析方法を開発した。この方法ではガラス試料をFe3+を還元するアスコルビン酸を共存させ分解することで、溶液中のFe3+とSn2+の酸化還元反応を防いだうえで、Sn2+とSn4+を分離し、ICP-AESでtotal SnおよびSn4+をそれぞれ定量する。本方法で得られたSn redoxはメスバウアー分光法で得られた値とよく一致することを確かめた。
さらに本方法とステップエッチング法を組み合わせることで、フロートガラスTin面から深さ方向のtotal SnおよびSn4+濃度プロファイルを分析するための新しい化学分析法を開発し、フロートガラスTin面表面からの深さ方向のtotal Sn、Sn4+、Sn2+、およびSn redoxの定量的な濃度プロファイルを得た。今回分析されたフロートガラス試料は、tin humpより浅い部分が還元層であること、tin humpより深い部分が酸化層であること、tin面の最表面は酸化していることを明らかとした。これらの結果は、先行研究の結果を支持した。さらに、最表面の最初のピークと、tin humpと一致する深さ7~8μmの2番目のピークからなる、複雑なSn4+濃度プロファイルを明らかにした。本方法は既存の方法よりも優れた深さ分解能を持つ、定量的な深さ方向のSnの価数別の分析方法である。本方法を活用することで、フロートガラスへのスズの侵入に関する詳細な情報を得ることができ、フロート法による高品質なガラスの製造に大きく貢献できる。
謝辞
本論文作成に際し、多大なご指導を賜った京都大学大学院工学研究科材料化学専攻三浦清貴教授、下間靖彦准教授、清水雅弘助教に、ここに謝意を表す。
参考文献
- Y. Arai, M. Inoue, K. Ishikawa, T. Yokote, Y. Kondo, K. Mori, Evolution of the glass light guide plate and its peripheral technologies for large size TV application, in: SID Symposium Digest of Technical Papers, 2017: pp. 1663–1666. https://doi.org/10.1002/sdtp.11964.
- W.A. Wely, Coloured Glasses, Society of Glass Technology, Sheffiled, 1981.
- M.R. Cicconi, A. Veber, D. de Ligny, J. Rocherullé, R. Lebullenger, F. Tessier, Chemical tunability of europium emission in phosphate glasses, J Lumin. 18 3(2017). https://doi.org/10.1016/j.jlumin.2016.11.019.
- G.H. Beall, Design and properties of glass-ceramics, Annual Review of Materials Science. 22(1992). https:// doi.org/10.1146/annurev.ms.22.080192.000515.
- D.B. Dingwell, Redox viscometry of some Fe-bearing silicate melts, American Mineralogist. 76(1991).
- D.B. Dingwell, Shear viscosities of ferrosilicate liquids, American Mineralogist. 74(1989).
- H. Tokunaga, Thermal conductivity measurement of glass melts and its applications, NEW GLASS. 34(2019)14–18.
- Y. Saijo, M. Murata, T. Kajihara, H. Hijiya, Y. Suzuki, R. Akiyama, M. Shimizu, Y. Shimotsuma, K. Miura, Speciation of tin ions in oxide glass containing iron oxide through solvent extraction and inductively coupled plasma atomic emission spectrometry after the decomposition utilizing ascorbic acid, Analytical Sciences. 38(2022)881–888. https://doi.org/10.1007/s44211-022-00110-w.
- S.D. Stookey, Coloration of glass by gold, silver, and copper, Journal of the American Ceramic Society. 32(1949)246–249. https://doi.org/10.1111/j.1151-2916.1949. tb18957.x.
- L. Skuja, Isoelectronic series of twofold coordinated Si, Ge, and Sn atoms in glassy SiO2: a luminescence study, J Non Cryst Solids. 149(1992)77–95. https://doi.org/10.1016/ 0022-3093(92)90056-P.
- ]K. Kim, Fining behavior in alkaline earth alumino borosilicate melts doped with As2O5 and SnO2, Journal of the American Ceramic Society. 96(2013)781–786. https:// doi.org/10.1111/jace.12188.
- A. Ellison, I.A. Cornejo, Glass Substrates for Liquid Crystal Displays, Int J Appl Glass Sci. 1(2010)87–103. https://doi.org/10.1111/j.2041-1294.2010.00009.x.
- J.S. Sieger, Chemical characteristics of float glass surfaces, J Non Cryst Solids. 19(1975)213–220. https://doi. org/10.1016/0022-3093(75)90086-1.
- R. Pyare, P. Nath, Simple and rapid spectrophotometric method for the determination of Tin(II)in binary alkali silicate glasses, Analyst. 110(1985)1321–1323. https://doi. org/10.1039/AN9851001321.
- J.E. Amonette, J. Matyáš, Determination of ferrous and total iron in refractory spinels, Anal Chim Acta. 910(2016)25–35. https://doi.org/10.1016/j.aca.2015.12.024.
- D.R.J. Jones, W.C. ansheski, D.S. Goldman, Spectrophoto metric Determination of Reduced and Total Iron in Glass with 1,10-Phenanthroline, Anal Chem. 53(1981)923–924. https://doi.org/10.1021/ac00229a049.
- R. Akiyama, N. Kanno, Y. Suzuki, K. Yamamoto, Deter mination of ferrous and total iron at the surface of float glass by spectrophotometry combined with a stepwise etching technique, Glass Technology - European Journal of Glass Science and Technology Part A. 56(2015)37–42.
- Y. Saijo, Y. Suzuki, M. Murata, R. Akiyama, M. Shimizu, Y. Shimotsuma, K. Miura, Separation and determination of sulfide sulfur and sulfate sulfur in soda lime silicate glass, J Non Cryst Solids. 571(2021)121072. https://doi.org/ 10.1016/j.jnoncrysol.2021.121072.
- H. Hijiya, Consideration on the structure of Fe2+ in system, NEW GLASS. 34(2019)14–17.
- H. Masai, Y. Suzuki, T. Yanagida, K. Mibu, Luminescence of Sn2+ center in ZnO-B2O3 glasses melted in air and Ar conditions, Bull Chem Soc Jpn. 88(2015)1047–1053. https://doi.org/10.1246/bcsj.20150145.
- D. Benne, C. Rüssel, M. Menzel, K.D. Becker, The effect of alumina on the Sn2+/Sn4+ redox equilibrium and the incorporation of tin in Na2O/Al2O3/SiO2 melts, J Non Cryst Solids. 337(2004)232–240. https://doi.org/10.1016/j. jnoncrysol.2004.04.017.
- K.F.E. Williams, C.E. Johnson, J.A. Johnson, D. Holland, M.M. Karims, Mössbauer spectra of tin in binary SiSn oxide glasses, Journal of Physics: Condensed Matter. 7(1995)9485–9497.
- K.F.E. Williams, C.E. Johnson, B.P. Tilley, D. Gelder, J.A. Johnson, Tin oxidation state, depth profiles of Sn2+ and Sn4+ and oxygen diffusivity in float glass by Mössbauer spectroscopy, J Non Cryst Solids. 211(1997)164–172. https://doi.org/10.1016/S0022-3093(96)00636-9.
- K.F.E. Williams, C.E. Johnson, O. Nikolov, M.F. Thomas, J.A. Johnson, J. Greengrass, Characterization of tin at the surface of float glass, J Non Cryst Solids. 242(1998)183–188. https://doi.org/10.1016/S0022-3093(98)00799-6.
- H. Masai, T. Ina, S. Okumura, K. Mibu, Validity of Valence Estimation of Dopants in Glasses using XANES Analysis, Sci Rep. 8(2018)415. https://doi.org/10.1038/s41598-017- 18847-0.
- A.M. Flank, P. Lagarde, J. Jupille, H. Montigaud, Redox profile of the glass surface, J Non Cryst Solids. 357(2011) 3200–3206. https://doi.org/10.1016/j.jnoncrysol.2011.03.046.
- M. Zheng, H. Wang, T. Haizheng, H. Yourong, J. Hong, The effect of tin on sulfur K-edge X-ray absorption near edge structure spectra of soda-lime-silicate glass: An experimental and comparative study, J Non Cryst Solids. 383(2014)71–74. https://doi.org/10.1016/j.jnoncrysol. 2013.04.027.
- Y. Gohshi, O. Hirao, I. Suzuki, Chemical state analysis of sulfur, chromium and tin by high resolution X-ray spectrometry, Advanced in X-Ray Analysis. 18(1974)406–414. https://doi.org/10.1154/S0376030800006911
- H. Masuda, Y. Fukumoto, K. Morinaga, Sn2+/Sn4+ Redox Equilibrium in the Oxide Glasses, Interdisciplinary Graduate School of Engineering Sciences, Kyushu University. 14(1992)173–179. https://doi.org/10.15017/ 17267.
- L. Jie, X. Chao, XPS examination of tin oxide on float glass surface, J Non Cryst Solids. 119(1990)37–40. https://doi. org/10.1016/0022-3093(90)90238-H.
- N. Kanno, M. Nakase, M. Harigai, Y. Saijo, R. Akiyama, K. Takeshita, The 35th Symposium on Ion Exchange & The 40th Symposium on Solvent Extraction, in: Approach to Determination of Fe2+/Fe3+ in Sn2+ Containing Glass by Solvent Extraction, Kitakyusyu, 2021: p. 82.
- O. Corumluoglu, E. Guadagnino, Determination of ferrous iron and total iron in glass by a colorimetric method, Glass Technology. 40(1999)24–28.
- A. Frankenberger, R.R. Brooks, M. Hoashi, Determination of vanadium in steels and geological materials by liquid- liquid extraction and graphite furnace atomic absorption spectrometry, Anal Chim Acta. 246(1991)359–363. https://doi.org/10.1016/S0003-2670(00)80973-3.
- K. Mikami, Volumetric determination of iron by ascorbic acid method, The Journal of the Japan Society for Analytical Chemistry. 27(1978)160–164. https://doi. org/10.2116/bunsekikagaku.27.3_160.
- P.F. Wyatt, Diethylammonium Diethyldithiocarbamate for the Separation and Determination of Small Amounts of Metals Part II. The Isolation and Determination of Arsenic, Antimony and Tin in Organic Compounds, Analyst. 80(1955)368–379.
- H. Goto, Y. Kakita, Photometric Determination of Tin in Iron and Steel(Ⅲ).Photometric Method with Sodiumdie thyldithiocarbamate and its Application to the Deterrni nation of Tin in Iron and Steel, Journal of the Japan Insti tute of Metals. 20(1956)319–322. https://doi.org/10.2320/ jinstmet1952.20.6_319.
- Y. Saijo, Y. Suzuki, R. Akiyama, M. Shimizu, Y. Shimotsuma, K. Miura, Speciation analysis of tin at the tin side of float glass by solvent extraction combined with a stepwise etching technique, J Non Cryst Solids. 592(2022). https:// doi.org/10.1016/j.jnoncrysol.2022.121752.
- L.A.B. Pilkington, The float glass process, Proc R Soc Lond A Math Phys Sci. 314(1969)1–25. https://doi. org/10.1098/rspa.1969.0212.
- T. Kloss, G. Lautenschlaeger, K. Schneider, Advances in the process of floating borosilicate glasses and some recent applications for specialty borosilicate float glasses, Glass Technology. 41(2000)177–181.
- K. Maeda, Glass Substrate for Flat Panel Displays, Journal of the Japan Society for Precision Engineering. 70(2004) 466–469. https://doi.org/10.2493/jjspe.70.466.
- K. Hayashi, J. Endo, S. Akiba, T. Nakashima, Novel damage-resistant glass for display cover, in: Proceedings of the International Display Workshops, 2011.
- J.S. Sieger, Chemical characteristics of float glass surfaces, J Non Cryst Solids. 19(1975)213–220. https://doi.org/ 10.1016/0022-3093(75)90086-1.
- Y. Hayashi, Y. Fukuda, M. Kudo, Investigation on changes in surface composition of float glass-mechanisms and effects on the mechanical properties, Surface Sciences. 507–510(2002)872–876. www.elsevier.com/locate/susc.
- Y. Hayashi, K. Matsumoto, M. Kudo, Mechanisms and chemical effects of surface tin enrichment on float glass, Glass Technology. 42(2001)130–133. https://www.scopus. com/inward/record.uri?eid=2-s2.0-0035435574&partnerID =40&md5=8bbc48e04a12d30b83cdd0addf68f9ed(accessed January 19, 2022).
- Y. Hayashi, R. Akiyama, M. Kudo, Surface characterization of float glass related to changes in the optical properties after reheating, Surface and Interface Analysis. 31(2001) 87–92. https://doi.org/10.1002/sia.960.
- G.H. Frischat, Tin ions in float glass cause anomalies, Comptes Rendus Chimie. 5(2002)759–763. https://doi. org/10.1016/S1631-0748(02)01436-4.
- K. F. E. Williams, M. F. Thomas, J. Greengrass, J. M. Bradshaw, Effect of tin on some physical properties of the bottom surface of float glass and the origin of bloom, Glass Technology. 40(1999)103–107.
- S. Takeda, Oxygen and silver diffusion into float glass, J Non Cryst Solids. 352(2006)3910–3913. https://doi.org/ 10.1016/j.jnoncrysol.2006.06.010.
- Y. Hayashi, K. Matsumoto, M. Kudo, The diffusion mechanism of tin into glass governed by redox reactions during the float process, J Non Cryst Solids. 282(2001) 188–196. https://doi.org/10.1016/S0022-3093(01)00319-2.
- G.H. Frischat, C. Müller-Fildebrandt, D. Moseler, G. Heide, On the origin of the tin hump in several float glasses, J Non Cryst Solids. 28 3(20 01)246–249 . https:// doi. org/10.1016/S0022-3093(01)00491-4.
- W. Meisel, Depth profile of tin in float glass - a CEMS study, Glass Science and Technology: Glastechnische Berichte. 72(1999)291–294.
- Y. Hayashi, K. Matsumoto, M. Kudo, The Diffusion Mechanism of Tin into Glass during the Float Process, Hyomen Kagaku. 22(2001)412–418. https://doi.org/ 10.1380/jsssj.22.412.
- A. Kumar, S.P. Singh, R. Pyare, Sn2+-Sn4+ and Fe2+-Fe3+ redox interaction in 30Na20-70 SiO2 glass, Glastech nische Berichte. 64(1991)106–108. http://www.bl.uk/ reshelp/atyourdesk/docsupply/help/terms/index.html.
- W.E. Baitinger, P.W. French, E.L. Swarts, Characterization of tin in the bottom surface of float glass by ellipsometry and XPS, J Non Cryst Solids. 38–39(1980)749–754.
- P.D. Townsend, N. Can, J. Chandler, B.W. Farmery, R. Lopez-Heredero, A. Peto, L. Salvin, D. Underdown, B. Yang, Comparisons of tin depth profile analyses in float glass, J Non Cryst Solids. 223(1998)73–85. https://doi.org/10.1016/S0022-3093(97)00348-7.
- J. A. Johnson, C. E. Johnson, K. F. E. Williams, D. Holland, M. M. Karim, Mössbauer spectra of tin in float glass, Hyperfine Interact. 95(1995)41–51.
- G. Principi, A. Maddalena, A. Gupta, F. Geotti-Bianchini, S. Hreglich, M. Veritá, Oxidation state of surface tin in an industrially produced float glass, Nuclear Inst. and Methods in Physics Research, B. 76(1993)215–217. https://doi.org/10.1016/0168-583X(93)95185-8.
- J.A. Johnson, C.E. Johnson, Mössbauer spectroscopy as a probe of silicate glasses, Journal of Physics Condensed Matter. 17(2005)R381–R412. https://doi.org/10.1088/ 0953-8984/17/8/R01.
- P.J. Potts, A handbook of silicate rock analysis2, in: Blackie, Glasgow, 1987.
- B. Bernas, A New Method for Decomposition and Comprehensive Analysis of Silicates by Atomic Absorp tion Spectrometry, Anal Chem. 40(1968)1682–1686. https://doi.org/10.1021/ac60267a017.
- D.E. Buckley, R.E. Cranston, Atomic absorption analyses of 18 elements from a single decomposition of alumino silicate, Chem Geol. 7(1971)273–284. https://doi.org/ 10.1016/0009-2541(71)90012-X.
- G.S. Collins, T. Kachnowski, N. Benczer- Koller, M. Pasternak, Application of the Mössbauer effect to the characterization of an amorphous tin-oxide system, Phys Rev B. 19(1979)1369–1373. https://doi.org/10.1103/ PhysRevB.19.1369.
- Q. Zhang, Z. Chen, Z. Li, Simulation of tin penetration in the float glass process(float glass tin penetration), Appl Therm Eng. 31(2011)1272–1278. https://doi.org/10.1016/ j.applthermaleng.2010.12.030.