AGC Research Report 68(2018)
Ethylene/Vinyl-fluoride Copolymerization using Organometallic Catalysts, and Olefin Insertion into a Pd-F bond for the Catalyst Reactivation
金属触媒を用いたエチレン/フッ化ビニル共重合及び触媒再活性化の鍵となるPd-F結合へのオレフィン挿入反応
和田真治*・Richard F. Jordan**
Shinji Wada*, Richard F. Jordan**
*AGC株式会社 商品開発研究所
**Department of Chemistry, The University of Chicago
金属触媒を用いた重合はポリマー構造を緻密に制御できる点で非常に有用である。例えばZiegler-Natta触媒やメタロセン触媒を用いることで、直鎖の高分子量ポリエチレンやアイソタクチックポリプロピレン、シンジオタクチックポリプロピレンなど、立体構造を制御したポリマーを合成することができる。一方、金属触媒を用いて含フッ素ポリマーの重合に成功した例は非常に少なく、ホスフィン-スルホナートパラジウム(Pd)触媒を用いてエチレンとフッ化ビニル及び3,3,3-トリフルオロプロペンを共重合した系が知られているのみであり、β-フッ素(β-F)脱離により生成する金属-F化合物の反応性が低い、などの理由から難易度が高いと考えられていた。
今回、配位子の構造が異なる数種類のホスフィン-スルホナートPd触媒を用いて、エチレンとフッ化ビニルの共重合を行い、その配位子の構造と得られたポリマーの組成や分子量の関係を考察した。得られたポリマーは過去のフッ化ビニル共重合検討と同様、フッ化ビニル導入量が1 mol%以下、Mwが3万以下のポリマーであった。しかしながら、ポリマー構造として、過去に観測されていない-CH2CHF2及び-CH2CH2F末端が観測された。このことは、β-F脱離によって生成したPd-F錯体に対してエチレン及びフッ化ビニルが挿入反応を起こした可能性を示唆していた。この仮説を検証するべく、ホスフィン-スルホナートPd-F錯体を合成し、フッ化ビニルとの反応を試みたところ、Pd-CH2CHF2錯体が得られた。またエチレンとの反応によって、末端に-CH2CH2F基を有するポリエチレンが得られた。これらの検証結果により、β-F脱離によって生成したPd-F錯体に対しオレフィンが挿入反応を起こし、重合が進行したことが確認された。この金属-F結合へのエチレン等非活性化オレフィン類の挿入反応は過去に報告例が無く、有用なフッ素化触媒反応に応用できる可能性がある。
Polymerization using organometallic catalysts is a powerful method for precise synthesis of structure controlled polymers. For example, high molecular weight linear polyethylene, and isotactic and syndiotactic polypropylene can be synthesized using Ziegler-Natta or metallocene catalysts. However, examples of the synthesis of fluorinated polymers using organometallic catalysts are rare. Only copolymerization of ethylene with vinyl fluoride or 3,3,3-trifluoropropene has been reported, and this is believed to be difficult for several reasons, including the low activity of metal-F compounds produced by β-F elimination.
In this work, we attempted to copolymerize ethylene with vinyl fluoride using phosphine-sulfonate Pd catalysts with several types of ligands, and the relationships between the ligand structure and polymer composition or molecular weight were evaluated. The obtained polymers were almost identical to those reported in previous papers on vinyl fluoride polymerization. They contained under 1 mol% vinyl fluoride, and their molecular weights were below 30,000, and novel terminal structures, ‒CH2CHF2 and ‒CH2CH2F, which have never previously been observed, were found. This implied that ethylene and vinyl fluoride could insert into Pd-F bond generated by β-F elimination. To confirm this hypothesis, a phosphine-sulfonate Pd-F complex was synthesized and reacted with vinyl fluoride, yielding a Pd-CH2CHF2 complex. The Pd-F complex was also reacted with ethylene to yield polyethylene with ‒CH2CH2F chain end. Based on these results, it was confirmed that ethylene and vinyl fluoride could insert into the Pd-F bond generated by β-F elimination, and that the polymerization proceeded. This is the first report on the insertion of unactivated olefins such as ethylene into a metal fluoride bond, and this insertion reaction could be applied to new and useful catalytic fluorination reactions.
1. 緒言
1.1. 金属触媒を用いた含フッ素ポリマーの重合
金属触媒を用いた重合はポリマー構造を緻密に制御できる点で有用である。例えばZiegler-Natta触媒を用いることによって、ラジカル重合では得られない、直鎖かつ高分子量の高密度ポリエチレン(HDPE)、アイソタクッチクポリプロピレン等を得ることができる。(1)またメタロセン触媒を用いることで、立体規則性の異なるアイソタクッチクポリプロピレン、シンジオタクチックポリプロピレンを作り分けることができる。(2)これらの金属触媒を用いた重合は、商業的に広く使われている方法である。その他にも様々な重合用金属触媒が開発され、その他の重合方法では合成できない構造のポリマーや、構造が制御されたポリマーが合成されている(3)。
一方、金属触媒を用いて含フッ素ポリマーの重合に成功した例は非常に少なく、ホスフィン-スルホナートPd触媒を用いてエチレンとフッ化ビニル及び3,3,3-トリフルオロプロペンを共重合した系が知られているのみである。(4)フッ化ビニル共重合体の検討例では、フッ化ビニル含有量が最大3.6 mol%、Mn(数平均分子量)が最大約10万程度のポリマーが得られ、3,3,3-トリフルオロプロペン共重合体の検討例では3,3,3-トリフルオロプロペン含有量が最大8.9 mol%、Mnが最大約10万程度のポリマーが得られている。これらの実験結果について、含フッ素モノマーの導入量が少なく、また触媒活性がエチレンの重合と比較して低下する理由はいくつか考察されており、①電子不足オレフィンである含フッ素オレフィンの金属中心への配位力が弱い、②電気陰性度の高いフッ素の効果により金属-Rf(Rf = 含フッ素アルキル基)結合が強固になることにより、反応中間体である金属-Rf錯体に対するオレフィン類の挿入反応が遅い、③金属-Rf錯体からβフッ素(β-F)脱離反応により生成する金属-F錯体の反応性が低く、触媒失活反応と成り得る、ことなどが考えられている(5)。
1.2. 金属-F化合物と炭素-炭素不飽和結合の反応
挿入反応などの、金属-F化合物と炭素-炭素不飽和結合(C=C, C≡C)の反応は金属-炭素結合の生成や炭素-F結合の生成に有用な手段である。例えば、アルカリ金属フッ化物、AgFやHgF2などの金属フッ化物と高度にフッ素化されたアルケン、アルキン類が反応することにより、フッ素化アルキル金属化合物やフッ素化アルケニル金属化合物が得られることが知られている(6,7)。また、Au-F錯体と内部アルキンの反応において、中心金属に配位したアルキンにフッ素アニオンが求核的に反応することで、内部アルキンにAu-Fがトランス付加した化合物が得られる(8)。さらに、アミノフッ素化反応やフルオロエステル化反応の鍵反応としてスチレンやアルキンのPd-F結合への挿入反応が提案されている(9-11)。その他、CS2がIr-F結合やPt-F結合に挿入することが報告されている(12)。
しかしながら、これまでエチレンなどの非活性化オレフィン類が金属-F結合に挿入する例は報告されていなかった。よって、1.1章で挙げた、金属触媒を用いた含フッ素モノマーの重合における課題③は、大きな問題となることが想定されていた。
1.3. 本研究の目的
本研究では、金属触媒を用いた含フッ素ポリマーの重合において、含フッ素モノマーの導入比率や触媒活性の向上を目指し、まず配位子構造の異なる数種類のホスフィンースルホナートPd触媒を用いてエチレン/フッ化ビニル共重合を行い、その配位子構造と得られたポリマーの組成や分子量の関係を考察し、触媒設計に活かすことを考えた。また考察を進める中で、β-F脱離反応によって生成したホスフィン-スルホナートPd-F錯体に対し、フッ化ビニル及びエチレンが挿入した可能性が示されたため、別途ホスフィン-スルホナートPd-F錯体を合成し、フッ化ビニル及びエチレンとの反応を試みることで、反応機構仮説の検証を行った。
本稿2章でまず、ホスフィン-スルホナートPd触媒を用いたエチレン/フッ化ビニル共重合について議論し、3章においてホスフィン-スルホナートPd-F錯体の合成及びその反応について議論する。
2. ホスフィン-スルホナートPd触媒を用いたエチレン/フッ化ビニル共重合検討
2.1. ホスフィン-スルホナートPd触媒
ホスフィン-スルホナートPd触媒は2002年にDrentらによって開発された触媒であり、一般的に金属触媒を用いた重合に適用しにくい含官能基オレフィン類の重合に有用な金属触媒である(13)。例えば、アクリル酸、アクリル酸メチル、酢酸ビニル、アクリロニトリル、ビニルエーテル、アクリルアミド、ビニルスルホン酸など様々なモノマーの重合検討が報告されている(Scheme 1)。
合成上、リン上の置換基R1, R2を変えることが容易であり、立体的および電子的特徴を持った様々なホスフィン-スルホナートPd触媒が合成され、その反応性の考察が行われている。
含フッ素オレフィンについては、フッ化ビニル、3,3,3-トリフルオロプロペンとエチレンの共重合の報告例があり(4)、ホスフィン-スルホナートPd触媒1~6が使用されている(Fig. 1)。
今回、触媒1~6とは配位子の構造が異なるホスフィン-スルホナートPd触媒7、8、9を用いて、エチレン/フッ化ビニル共重合検討を行った(Fig. 2)。触媒7はエチレン/メチルアクリレート共重合体において高活性を示した触媒であり(14)、触媒8はエチレンの単独重合において高活性かつ高い分子量のポリエチレンを生成した触媒である(15)。触媒9はエチレン単独重合において高活性かつエチレン/ビニルエーテル共重合において高活性を示した触媒である(16)。
エチレン/フッ化ビニル共重合において、配位子の構造と得られるポリマーの組成や分子量の相関を考察し、高い含フッ素モノマー導入比率及び高い重合活性を示す触媒を設計することを目的とし、これらの触媒を用いて重合を行い、過去報告された重合結果と比較した。
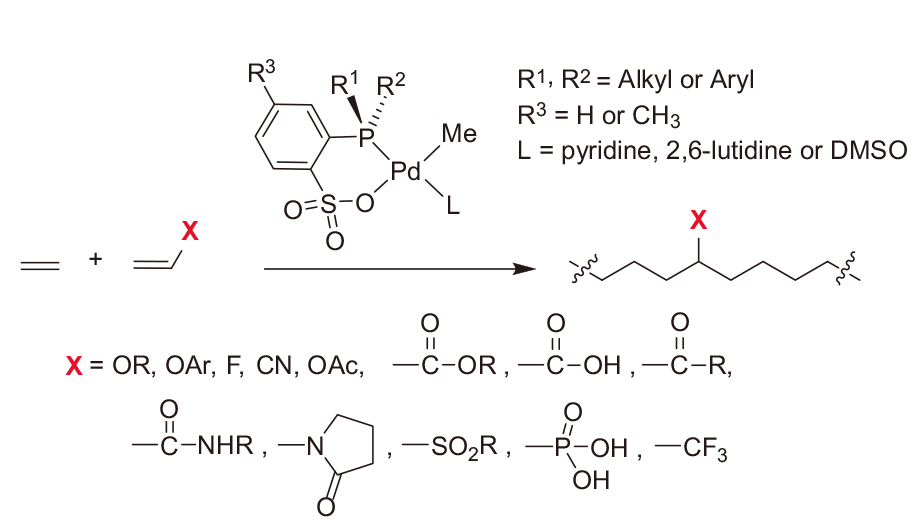 Scheme 1. Polymerization of functionalized olefins with
Phosphine-Sulfonate Pd catalysts.
Scheme 1. Polymerization of functionalized olefins with
Phosphine-Sulfonate Pd catalysts.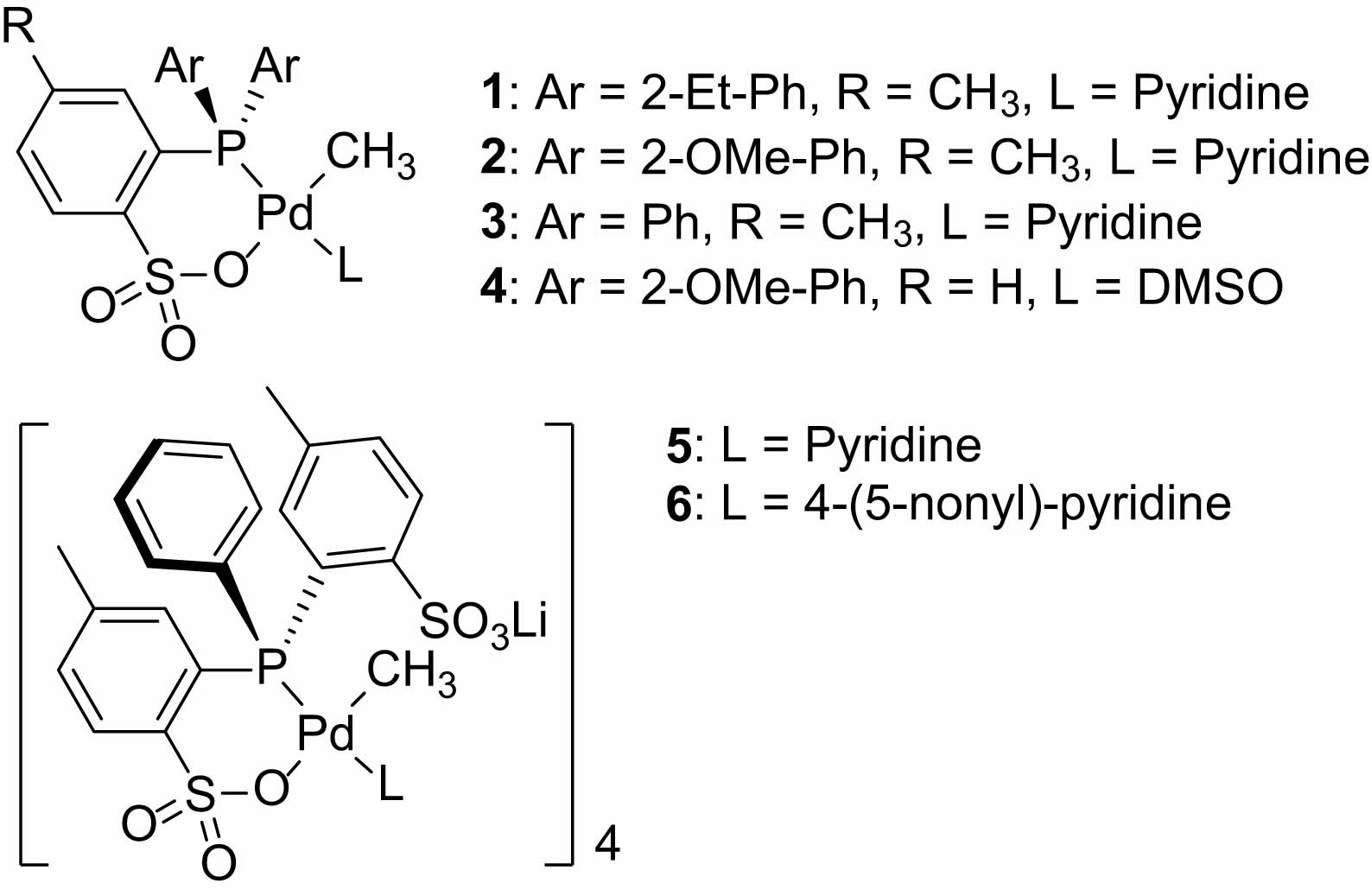 Fig. 1. Phosphine-Sulfonate Pd catalysts used for the
copolymerization of Ethylene/Vinyl fluoride,
3,3,3-trifluoropropene.
Fig. 1. Phosphine-Sulfonate Pd catalysts used for the
copolymerization of Ethylene/Vinyl fluoride,
3,3,3-trifluoropropene. 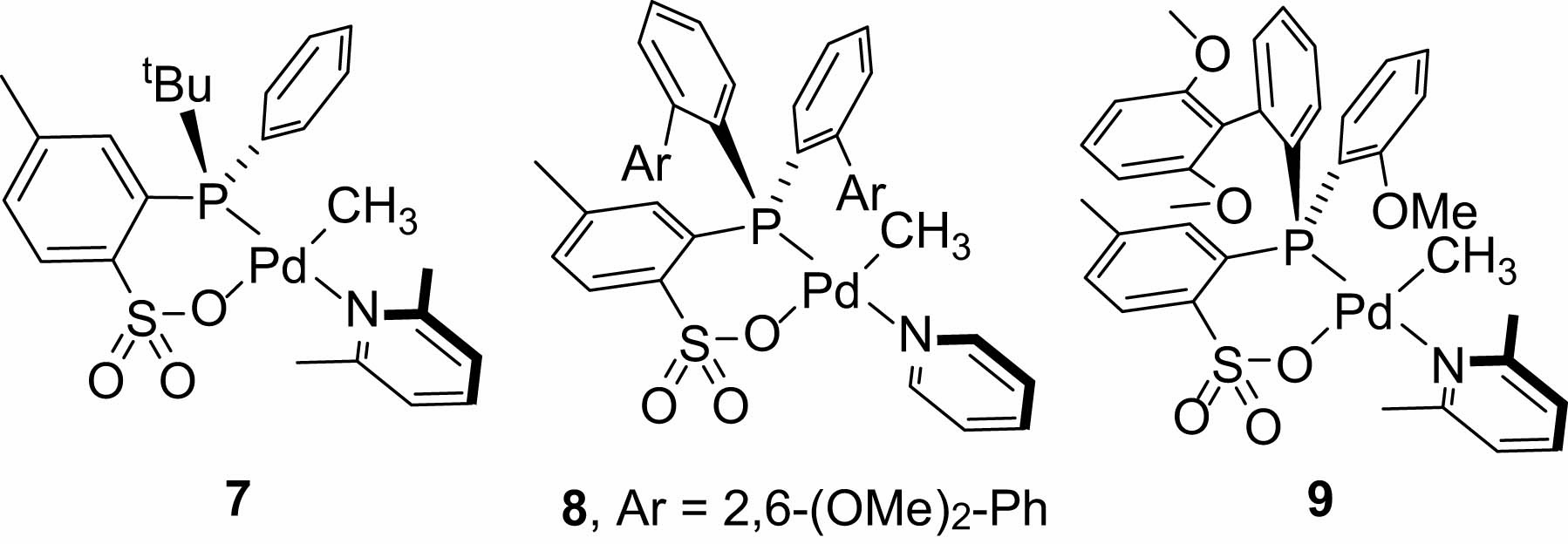 Fig. 2. Catalysts for the copolymerization of Ethylene/Vinyl
fluoride.
Fig. 2. Catalysts for the copolymerization of Ethylene/Vinyl
fluoride.2.2. 実験
触媒2(リファレンス)、7~9を用いた重合検討は以下のように行った(Scheme 2)。グローブボックス内で200 mLビーカーに40 mLのトルエンを仕込み、300 mLのステンレス製オートクレーブ(メカニカルスターラーと水冷チューブが接続されている)中に置いて密閉した。オートクレーブをグローブボックス外に取り出し、撹拌・温度コントローラーに接続したのち、0.55 MPaのフッ化ビニルと1.52 MPaのエチレンをオートクレーブ中に導入した(全圧2.07 MPa)。撹拌回転数170 rpm、温度80 ℃に設定し、温度が80 ℃に到達したタイミングで、グローブボックス内で別途耐圧容器中に調製した触媒10 μmolのクロロベンゼン10 mL溶液をN2ガスでオートクレーブ中に圧送した(全圧2.41 MPa)。重合中、エチレンを連続添加した。2hr後冷却し、ビーカー内に生成したポリマーを300 mLのアセトンで再沈したのちろ過にて回収し、10 mLのアセトンで3回洗浄、ろ過したのち、70 ℃真空オーブンで一晩乾燥を行い、目的のエチレン/フッ化ビニル共重合体を得た(Scheme 2)。
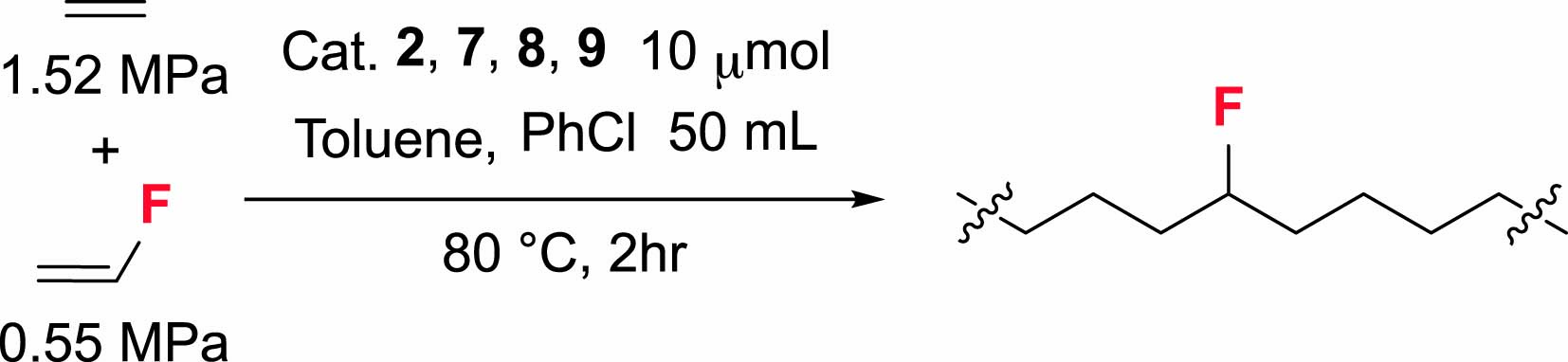 Scheme 2. Procedure of the copolymerization of Ethylene/
Vinyl fluoride.
Scheme 2. Procedure of the copolymerization of Ethylene/
Vinyl fluoride.2.3. 結果
重合結果をTable 1に示す。
触媒2、7、8、9すべてにおいて直鎖のエチレン/フッ化ビニル共重合体が得られ、フッ化ビニルの導入量は0.34~0.55 mol%であった。この結果は触媒1~3で過去検討された結果と同等であった。触媒8が最も高活性の触媒であり、リファレンス触媒2と比較して約25倍高活性であった。また触媒7は、フッ化ビニル導入量は最も低い(0.34 mol%)が、分子量の最も高い共重合体を生成した。
得られたエチレン/フッ化ビニル共重合体の部分構造をTable 2に示す。触媒2及び7で合成された共重合体においては75 %以上のフッ化ビニルが、-CH2CHFCH2-という形で導入されており、これは触媒1~3の重合結果と類似の結果であった。一方、触媒8、9を用いて合成された共重合体においては、過去の検討では観測されなかった、-CH2CHF2(major)と-CH2CH2F(minor)末端構造が観測された。これらの構造は、今回触媒2、7を用いた際も少量観測された。
新たに観測された末端構造はNMRによって同定された。(Fig. 3)
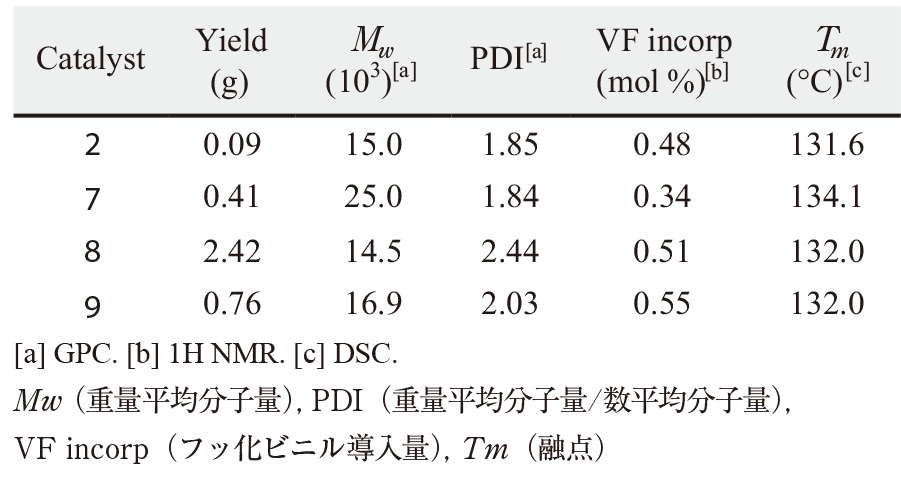
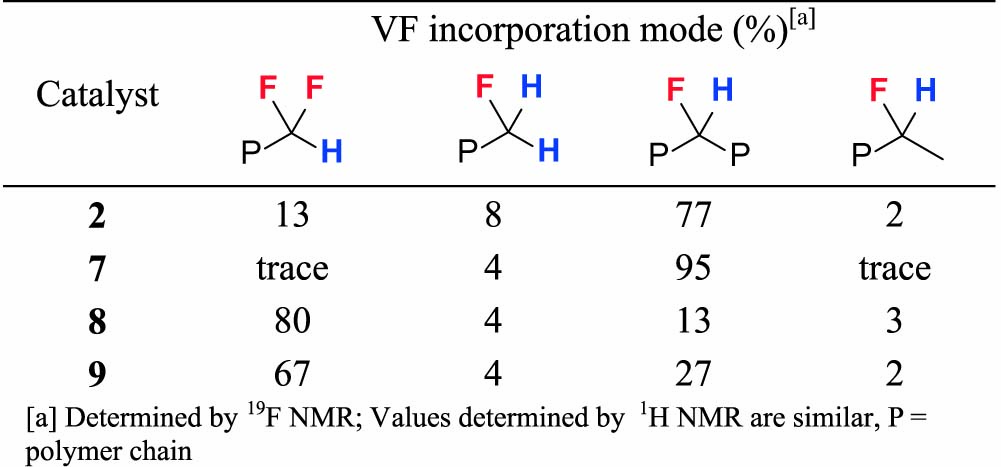
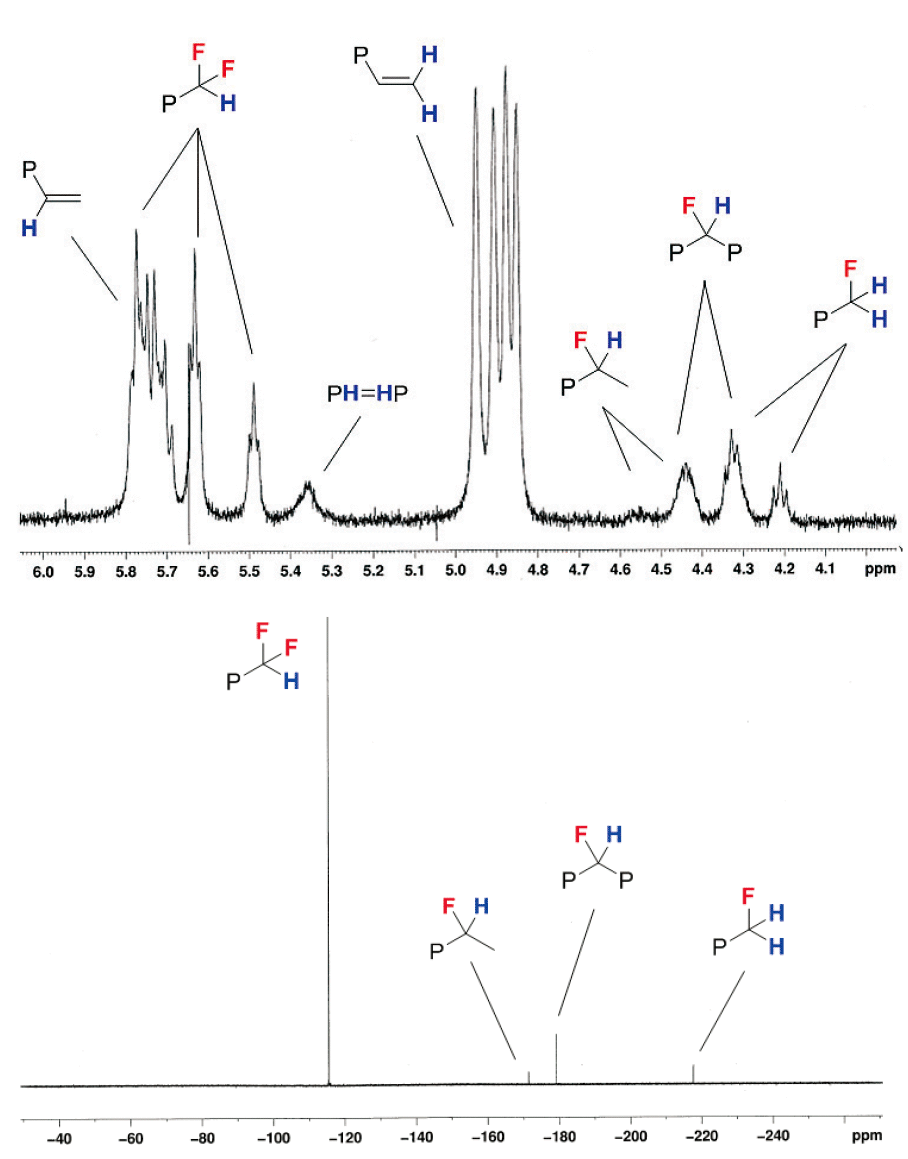 Fig. 3. 1H NMR (former, δ 6.0 to 4.0 region, 120 ℃) and
{1H} 19F NMR (latter, 100 ℃) spectra of the
copolymer produced by catalyst 8. Solvent:
o-dichlorobenzene-d4
Fig. 3. 1H NMR (former, δ 6.0 to 4.0 region, 120 ℃) and
{1H} 19F NMR (latter, 100 ℃) spectra of the
copolymer produced by catalyst 8. Solvent:
o-dichlorobenzene-d42.4. 考察(–CHF2、-CH2 F末端生成機構仮説及び検証)
今回、これら-CH2CHF2末端、-CH2CH2F末端が生成した機構としてラジカル機構を疑い、ガルビノキシルフリーラジカルを添加したラジカル阻害条件で触媒8を用いて重合を行ったが、同じ末端構造が観測された。また、原料であるフッ化ビニルに微量のフッ化ビニリデンが混入し、それがこれら末端構造の要因となった可能性を考え、触媒8を用いてフッ化ビニリデンの重合を試みたが、得られた共重合体中の-CH2CHF2末端構造の量は増加しなかった。もう一つの仮説として、反応中間体として存在するPd-CH2CHF-R種やPd-CH(CH2F)-R種から、β-F脱離反応により生成するPd-F錯体に対し、フッ化ビニルやエチレンが挿入し、重合が進行するということが考えられた。この仮説を検証するために、ホスフィン-スルホナートPd-F錯体11を合成し、フッ化ビニルやエチレンとの反応を試みた。
3. Pd-F結合へのオレフィン挿入反応
3.1. ホスフィン-スルホナートPd-F錯体の合成
3.1.1. 実験と結果
ホスフィン-スルホナートPd-F錯体11はホスフィン-スルホナートPd-Br錯体10にCH2Cl2中AgFを反応させることによって合成することができた。ホスフィン-スルホナートPd-Br錯体10は(COD)PdBr2錯体に対し、配位子前駆体であるH[POBp, OMe] (= H[P(2-OMe-Ph)(2-{2,6-(OMe)2-Ph}-Ph)(2-SO3-5-MePh)])及び2,6-lutidine(lut)を反応させることによって合成した(Scheme 3)。
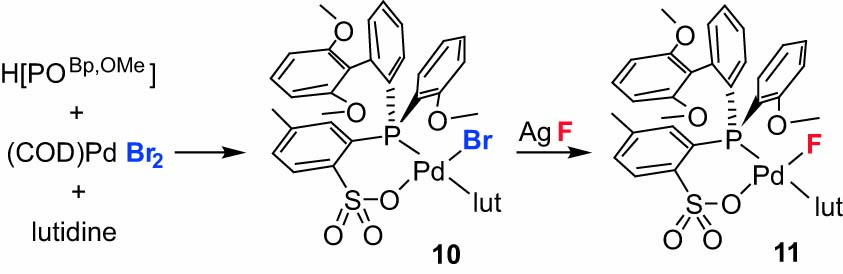 Scheme 3. Synthesis of Phosphine-Sulfonate Pd-F
complex 11.
Scheme 3. Synthesis of Phosphine-Sulfonate Pd-F
complex 11.Pd-F錯体11はCH2Cl2中で再結晶することによって、11・3CH2Cl2という形で結晶が得られ、X線結晶構造解析によって分析した(Fig. 4)。
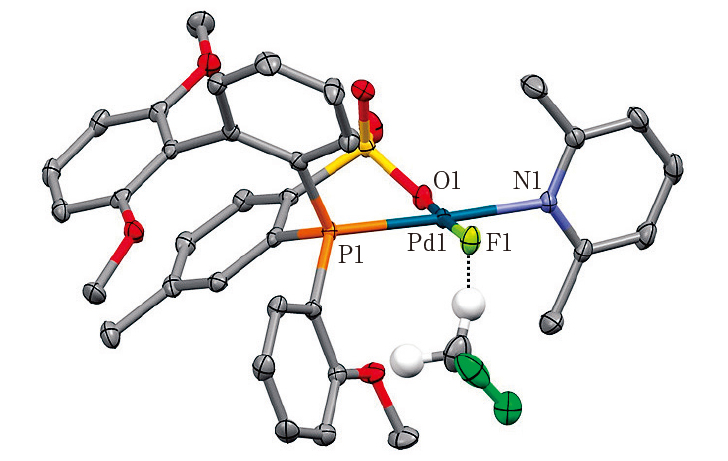 Fig. 4. Molecular structure of 11•3CH2Cl2. H atoms and
two CH2Cl2 molecules are omitted. Selected bond
lengths (Å): Pd1-F1 1.9476(14), Pd1-O1 2.0171
(17), Pd1-N1 2.112(2), Pd1-P1 2.2466(6),
F---HCHCl2 2.090.
Fig. 4. Molecular structure of 11•3CH2Cl2. H atoms and
two CH2Cl2 molecules are omitted. Selected bond
lengths (Å): Pd1-F1 1.9476(14), Pd1-O1 2.0171
(17), Pd1-N1 2.112(2), Pd1-P1 2.2466(6),
F---HCHCl2 2.090.3.1.2. 考察
結晶中に含まれているCH2Cl2の水素原子とPd-F原子との距離が2.090 Åであり(Fig. 4中点線)、H-F水素結合を形成していることが確認された。
31P{1H}NMRスペクトル(CD2Cl2)においてはδ-4.0にダブレット(JPF = 17 Hz)が観測された(Fig.5)。また、19F{1H}スペクトルにおいてはδ -429.3にブロードニングしたシングレットが観測された(Fig.6)。本来P-Fカップリングにより、ダブレットとして観測されるはずであるが、微量含まれていたH2OやHFとのH-F水素結合によって、ブロードニングしたと推測している。実際、H2O及びHFのスカベンジャーとして乾燥CsFを添加して19F{1H}NMRを測定すると、同じ位置にダブレットが観測され、そのJPFは17Hzであった(17)(Fig. 7)。
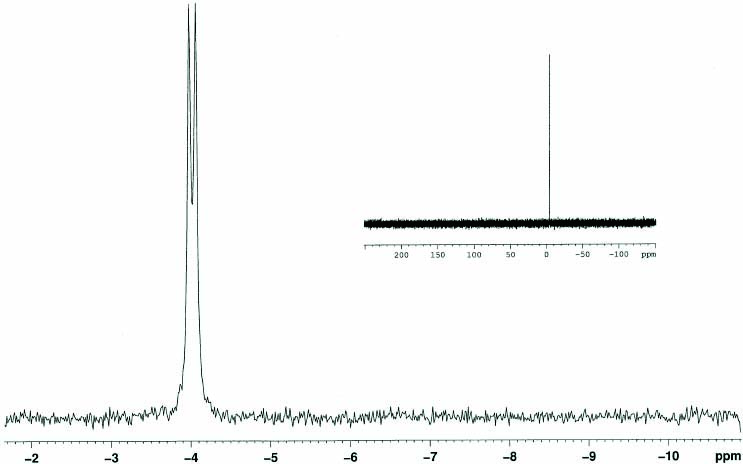 Fig. 5. 31P{1H}NMR spectrum of Pd-F complex 11(CD2Cl2).
Fig. 5. 31P{1H}NMR spectrum of Pd-F complex 11(CD2Cl2). 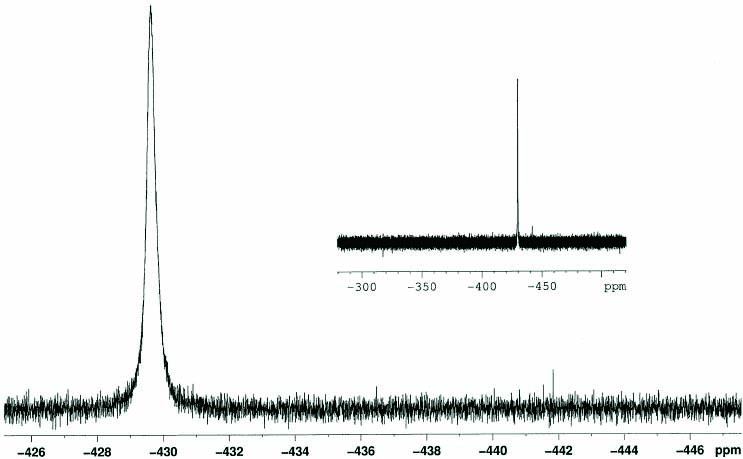 Fig. 6. 19F{1H} NMR spectrum of Pd-F complex 11 without
CsF (CD2Cl2).
Fig. 6. 19F{1H} NMR spectrum of Pd-F complex 11 without
CsF (CD2Cl2).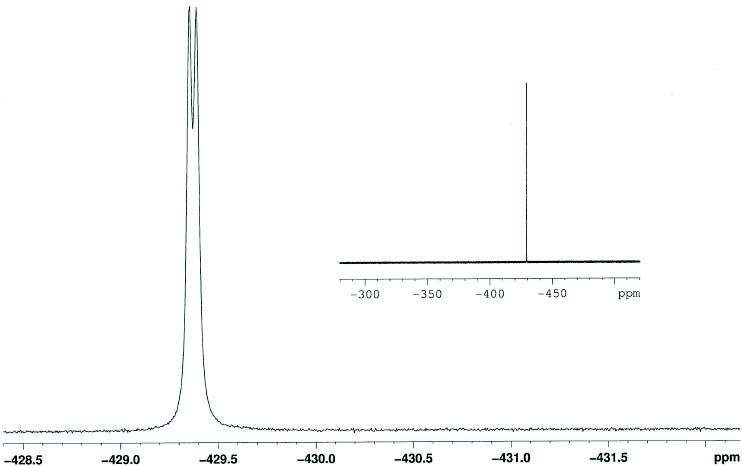 Fig. 7. 19F{1H} NMR spectrum of Pd-F complex 11 with CsF
(CD2Cl2).
Fig. 7. 19F{1H} NMR spectrum of Pd-F complex 11 with CsF
(CD2Cl2).3.2. ホスフィン-スルホナートPd-F錯体11とフッ化ビニル及びエチレンの反応
3.2.1. 実験と結果
合成したホスフィン-スルホナートPd-F錯体11とフッ化ビニル及びエチレンとの反応を試みた。Pd-F錯体11とフッ化ビニル(0.19 MPa)をCH2Cl2中、室温で24時間反応させるとPd-F結合に対してフッ化ビニルが挿入して生成した錯体、(POBp, OMe)Pd(CH2CHF2)(lut) (1 2)が収率37 %で得られた。Pd-F錯体11はエチレンとも反応し(CH2Cl2、0.36MPa、r.t)、末端に-CH2CH2F基を有するポリエチレンが得られた。これはエチレンがPd-F結合に挿入し、重合反応が進行したことを示す。また、Pd-CH2CHF2錯 体1 2はフッ化ビニルとは反応しなかったが(CH2Cl2、0.20 MPa、r.t.)、エチレンとは反応し(CH2Cl2、0.26 MPa、r.t.)、末端に-CH2CHF2を有するポリエチレンが生成した(Scheme 4)。
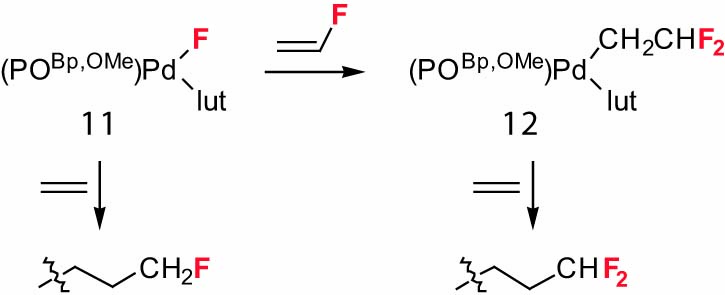 Scheme 4. Reaction of Phosphine-Sulfonate Pd-F complex
11 with Ethylene and Vinyl fluoride.
Scheme 4. Reaction of Phosphine-Sulfonate Pd-F complex
11 with Ethylene and Vinyl fluoride.3.2.2. 考察
(POBp, OMe)Pd(CH2CHF2)(lut) (12)の1H NMRスペクトル(C6D5Cl、60 ℃)においてPd-CH2CHF2に対応するシグナルがδ 5.11にtt (JHF = 59 Hz、JHH= 5 Hz)として観測され、Pd-CH2CHF2に対応するシグナルがδ 1.26にマルチプレットとして観測された(Fig. 8)。また、これらのシグナルはHH COSYスペクトルにおいて相関が見られた。19F{1H}スペクトルにおいて、Pd-CH2CHF2に対応するシグナルがδ-96.1及びδ -99.3にそれぞれダブレット(JFF = 195Hz)として観測された(Fig. 9)。これは同一炭素上にある2つのジアステレオトピックなF原子に対応するシグナルとして帰属できる。
またCH2Cl2で再結晶することにより、12・CH2Cl2という形で結晶が得られ、X線結晶構造解析によって分析した(Fig. 10)。
Pd-CH2CHF2錯体12は60 ℃でβ-F脱離反応を起こし、Pd-F錯体11とフッ化ビニルを生成した。錯体12からのβ-F脱離反応はより極性の高い溶媒を使用した場合に速く、C6D5Cl中ではPd-F錯体11及びフッ化ビニルの生成は1 %であったが、CDCl2CDCl2中では10%であった(60 ℃保持、15 min後にNMRを測定)。このことは、β-F脱離反応を抑制するためには、非極性溶媒を使用した方が良い可能性を示している。
このように、ホスフィン-スルホナートPd-F錯体に対してフッ化ビニル及びエチレンが挿入することを新たに見いだした。特徴的な末端構造(-CH2CHF2,-CH2CH2F末端)を与えるホスフィン-スルホナートPd触媒を用いたエチレン/フッ化ビニル共重合系では、β-F脱離反応によって生成したPd-F錯体へのフッ化ビニル、エチレン挿入を鍵とする重合反応機構が強く示唆される。
4. 総括
ホスフィン-スルホナートPd触媒7、8、9を用いて、エチレン/フッ化ビニル共重合検討を行った。触媒8は過去に検討されたホスフィン-スルホナートPd触媒2と比較して約25倍程度の高活性を発現した。また、得られたエチレン/フッ化ビニル共重合体は新規な-CH2CHF2末端及び-CH2CH2F末端を有することを見出した。
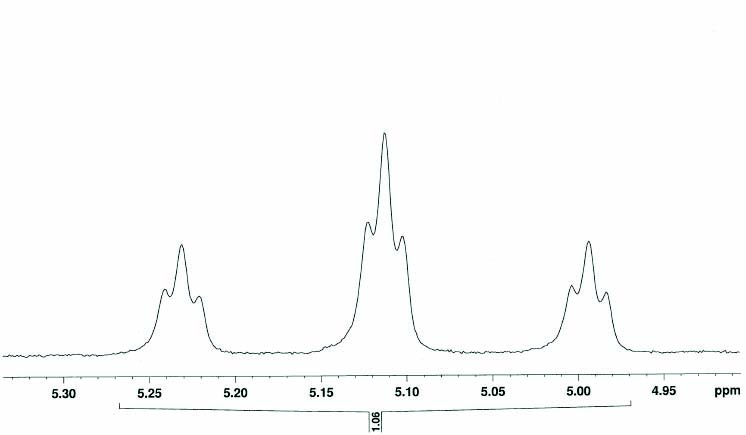
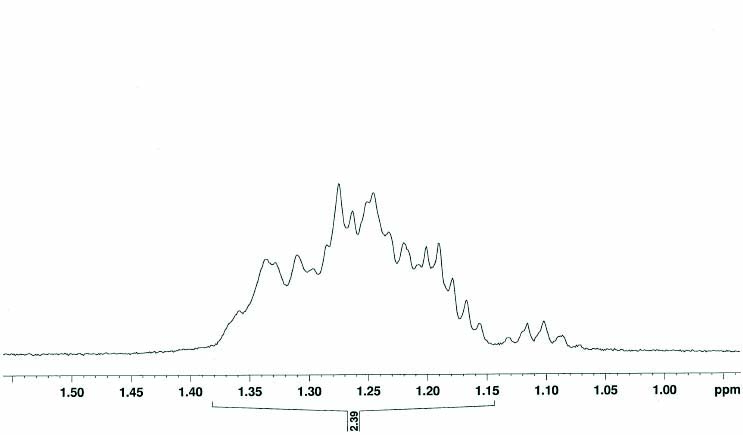 Fig. 8. 1H NMR spectrum of Pd-CH2CHF2 complex 12
(C6D5Cl, 60 ℃).
Fig. 8. 1H NMR spectrum of Pd-CH2CHF2 complex 12
(C6D5Cl, 60 ℃).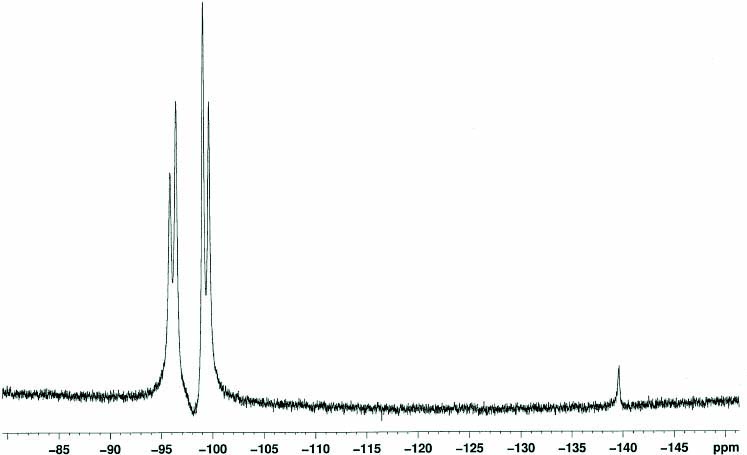 Fig. 9. 1H NMR spectrum of Pd-CH2CHF2 complex 12
(C6D5Cl, r.t.). The signal around δ -140 may be
corresponding to [SiF62-
].
Fig. 9. 1H NMR spectrum of Pd-CH2CHF2 complex 12
(C6D5Cl, r.t.). The signal around δ -140 may be
corresponding to [SiF62-
].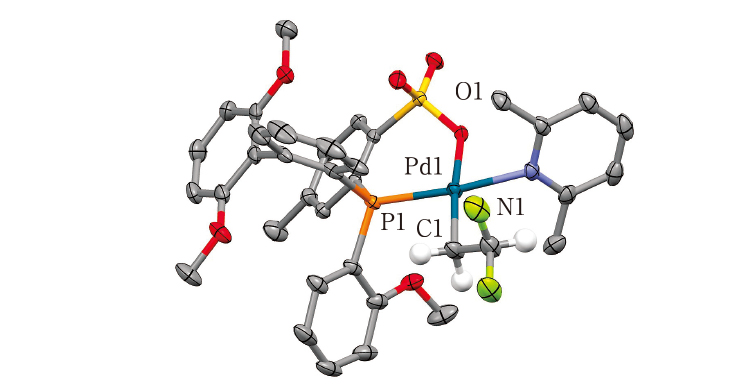 Fig. 10. Molecular structure of 12. H atoms and a CH2Cl2molecule are omitted. Selected bond lengths(Å):
Pd1-C1 2.045(2), Pd1-O1 2.1277(15), Pd1-N1
2.1337(18), Pd1-P1 2.2459(6).
Fig. 10. Molecular structure of 12. H atoms and a CH2Cl2molecule are omitted. Selected bond lengths(Å):
Pd1-C1 2.045(2), Pd1-O1 2.1277(15), Pd1-N1
2.1337(18), Pd1-P1 2.2459(6).ホスフィン-スルホナートPd-F錯体11の合成に成功し、フッ化ビニルとの反応により、Pd-F結合にフッ化ビニルが挿入したPd-CH2CHF2錯体12が、一方、エチレンとの反応により、-CH2CH2F末端を有するポリエチレンが生成することを明らかにした。さらに、Pd-CH2CHF2錯体12はエチレンと反応し、-CH2CHF2末端を有するポリエチレンが生成することを見出した。これらの結果は、ホスフィン-スルホナートPd触媒を用いたエチレン/フッ化ビニル共重合おいては、β-F脱離反応により生成したPd-F錯体にフッ化ビニル及びエチレンが挿入し、重合反応が進行していることを強く示唆している。本反応の推定反応機構をScheme 5に示す。
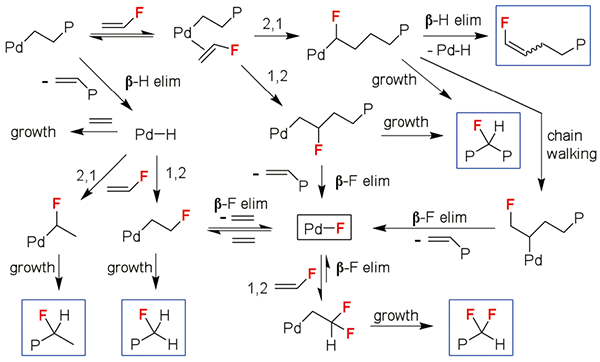 Scheme 5. Proposed mechanism of the copolymerization
of Ethylene/Vinyl fluoride by PhosphineSulfonate
Pd catalyst.
Scheme 5. Proposed mechanism of the copolymerization
of Ethylene/Vinyl fluoride by PhosphineSulfonate
Pd catalyst.これまで、金属-F結合にエチレンなどの非活性化オレフィン類が挿入した例は無く、金属触媒を用いた含フッ素ポリマーの重合においては、β-F脱離反応は触媒失活反応と成り得ると考えられていた。しかし、今回の実験結果により、ホスフィン-スルホナートPd触媒においては、触媒失活反応ではないことが示された。また、このPd-F錯体への非活性化オレフィンの挿入反応が、有用な触媒的フッ素化反応に応用できる可能性があると考えている。本研究はAngew. Chem.Int. Ed. 2017, 56, 1820. にまとめられており、そちらも参照していただきたい。
5. 謝辞
本研究は私がThe University of Chicago留学時代に検討した内容であり、私を指導してくださった、Richard F. Jordan教授に謝意を表します。また、研究室生活の様々な面で私を助けてくれた、Jordan研究室の学生達、Department of Chemistryのスタッフ達に謝意を表します。
参考文献
- John Jr. Boor et al., “Ziegler-Natta Catalysts Polymerizations 1st Edition”, (1979) Academic Press.
- G. G. Hlatky et al., “Olefin Polymerization by Metallocene Catalysts”, (2016) John Wiley & Sons, Inc
- R. Hoff, R. T. Mathers et al., “Handbook of Transition Metal Polymerization Catalysts”, (2010) John Wiley & Sons, Inc.
- Vinyl Fluoride: a) W. Weng, Z. Shen, R. F. Jordan, J. Am. Chem. Soc. 129 15450 (2007). b) Z. Shen, R. F. Jordan, J. Macromolecules 43 8706 (2010). 3,3,3-trifluoropropene: c) B. Rieger et al., ACS Macro Lett. 3 931 (2014).
- S. Wada, R. F. Jordan, Angew. Chem. Int. Ed. 56 1820(2017).
- Alkali metals: a) W. T. Miller, Jr., J. H. Fried, H. Goldwhite, J. Am. Chem. Soc. 82 3091 (1960); b) A. E. Bayliff, R. D. Chambers, J. Chem. Soc., Perkin Trans. 1, 201 (1988); c) B. V. Nguyen, J. Burton, J. Org. Chem. 62 7758 (1997); d) R. D. Chambers, T. Nakamura, J. Chem. Soc., Perkin Trans. 1, 398 (2001). Ag: e) W. T. Miller, Jr., M. B. Freedman, J. H. Fried, H. F. Koch, J. Am. Chem. Soc. 83 4105(1961); f) W. T. Miller, Jr., R. J. Burnard, J. Am. Chem. Soc . 90 7367 (1968); g) W. T. Miller, R. H. Snider, R. J. Hummel, J. Am. Chem. Soc . 91 6532 (1969); h) R. E. Banks, R. N. Haszeldine, D. R. Taylor, G. Webb, Tetrahedron Lett.5215 (1970); i) B. L. Dyatkin, B. I. Martynov, L.G. Martynova, N. G. Kizim, S. R. Sterlin, Z. A. Stumbrevichute,L. A. Fetorov, J. Organnomet. Chem. 57 423 (1973).Hg: j) C. G. Krespan, J. Org. Chem. 25 105 (1960); k) P. E.Aldrich, E. G. Howard, W. J. Linn, W. J. Middleton, W. H. Sharkey, J. Org. Chem. 28 184 (1963); l) W. T. Miller, M. D. Freedman, J. Am. Chem. Soc. 85 180 (1963); m) B. L. Daytkit, S. R. Sterlin, B. I. Martynov, E. I. Mysov, I. L. Knunyants, Tetrahedron 27 2843 (1971).
- a) A. Probst, K. Raab, K. Ulm, K. von Werner, J. Fluorine Chem. 37 223 (1987); b) C.-C. Lee, S.-T. Lin, J. Chem. Research142 (2000); c) R. Loska, M. Makosza, J. Org. Chem. 72 1354 (2007); d) L. Zhu, Y. Li, Y. Zhao, J. Hu, Tetrahedron Letters 51 6150 (2010); e) P. J. Riss, F. I. Aigbirhio, Chem. Comm. 47 11873 (2011); f) P. J. Riss, V. Ferrari, L. Brichard, P. Burke, R. Smith, F. I. Aigbirhio, Org. Biomol. Chem. 10 6980 (2012); g) B. Gao, Y. Zhao, C. Ni, J. Hu, Org. Lett. 16 102 (2014); h) A. Hafner, T. J. Feuerstein, S. Brase, Org. Lett. 15 3468 (2013); i) A. Hafner, N. Jung, S. Brase, Synthesis, 46 1440 (2014); j) B. Gao, Y. Zhao, J. Hu, Angew. Chem. Int. Ed. 54 638 (2015); Angew. Chem. 127 648 (2015); k) X. Wang, Y. Li, Y. Guo, Z. Zhu, Y. Wu, W. Cao, Org. Chem. Front 3 304 (2016); l) Y. Li, X. Wang, Y. Guo, Z. Zhu, Y. Wu, Y. Gong, Chem. Commun . 52 796 (2016).
- J. A. Akana, K. X. Bhattacharyya, P. Müller, J. P. Sadighi, J. Am. Chem. Soc. 129 7736 (2007).
- a) S. Qiu, T. Xu, J. Zhou, Y. Guo, G. Liu, J. Am. Chem. Soc. 132 2856 (2010); b) H. Peng, Z. Yuan, H. Wang, Y. Guo, G. Liu, Chem. Sci. 4 3172 (2013).
- H. Peng, G. Liu, Org. Lett. 13 772 (2011).
- Olefin insertion into M-N and M-O bonds: P. S. Hanley, J. F. Hartwig, Angew. Chem. Int. Ed. 52 8510 (2013)
- a) P. Kläring, T. Braun, Angew. Chem. Int. Ed. 52 11096 (2013); b) J. A. Evans, M. J. Hacker, R. D. W. Kemmitt, D. R. Russell, J. Stocks, J. Chem. Soc., Chem. Commun.72 (1972).
- A. Nakamura, T. M. J. Anselment, J. Claverie, B. Goodall, R. F. Jordan, S. Mecking, B. Rieger, A. Sen, P. W. N. M. van Leeuwen, K. Nozaki, Acc. Chem. Res. 46 1438 (2013)
- L. Piche, J. Daigle, G. Rehse, J. P. Claverie, Chem. Eur. J. 18 3277 (2012).
- K. M. Skupov, P. R. Marella, M. Simard, G. P. A. Yap, N. Allen, D. Conner, B. L. Goodall, J. P. Claverie, Macromol. Rapid Commun. 28 2033 (2007).
- J. D. Defoe, “Ph.D. Thesis, University of Chicago”, (2011).
- a) D. Y. Yandulov, N. T. Tran, J. Am. Chem. Soc. 129 1342 (2007). b) C. J. Bourgeois, S. A. Garratt, R. P. Hughes, R. B. Larichev, J. M. Smith, A. J. Ward, S. Willemsen, D. Zhang, A. G. DiPasquale, L. N. Zakharov, A. L. Rheingold, Organometallics 25 3474 (2006).